题目内容
绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途,在某些食品中可取代或部分取代目前常用的人工合成的抗氧化剂.

(1)在反应①中,绿原酸与水按1:1发生反应,则绿原酸的分子式为 ,反应①反应类型为
(2)1mol化合物I与足量金属钠反应生成标准状况下氢气体积为
(3)写出化合物II 与浓溴水反应的化学反应方程式: .
(4)1mol化合物II 与足量的试剂X反应得到化合物III ( ),则试剂x是
),则试剂x是
(5)化合物Ⅳ有如下特点:①与化合物II互为同分异构体;②遇FeCl3溶液显色;③1mol 化合物Ⅳ与足量银氨溶液反应生成4mol Ag;④苯环上的一卤代物只有一种.写出化合物Ⅳ的一种可能的结构简式 .

(1)在反应①中,绿原酸与水按1:1发生反应,则绿原酸的分子式为
(2)1mol化合物I与足量金属钠反应生成标准状况下氢气体积为
(3)写出化合物II 与浓溴水反应的化学反应方程式:
(4)1mol化合物II 与足量的试剂X反应得到化合物III (
 ),则试剂x是
),则试剂x是(5)化合物Ⅳ有如下特点:①与化合物II互为同分异构体;②遇FeCl3溶液显色;③1mol 化合物Ⅳ与足量银氨溶液反应生成4mol Ag;④苯环上的一卤代物只有一种.写出化合物Ⅳ的一种可能的结构简式
考点:有机物的推断,同分异构现象和同分异构体
专题:有机物的化学性质及推断
分析:(1)从质量守恒的角度确定绿原酸的分子式;
(2)化合物I含有4个-OH和1个-COOH,都可与钠反应生成氢气;
(3)化合物II含有酚羟基,可与浓溴水发生取代反应,含有碳碳双键,可与溴水发生加成反应;
(4)对比化合物II和化合物Ⅲ,可知化合物II应和酸性比-COOH弱,但比酚羟基强的酸对应的盐反应;
(5)①与化合物II互为同分异构体;②遇FeCl3溶液显色,说明分子中含有酚羟基;③1mol 化合物Ⅳ与足量银氨溶液反应生成4mol Ag,说明分子中含有2个醛基;④苯环上的一卤代物只有一种,可能含有1个可被取代的H.
(2)化合物I含有4个-OH和1个-COOH,都可与钠反应生成氢气;
(3)化合物II含有酚羟基,可与浓溴水发生取代反应,含有碳碳双键,可与溴水发生加成反应;
(4)对比化合物II和化合物Ⅲ,可知化合物II应和酸性比-COOH弱,但比酚羟基强的酸对应的盐反应;
(5)①与化合物II互为同分异构体;②遇FeCl3溶液显色,说明分子中含有酚羟基;③1mol 化合物Ⅳ与足量银氨溶液反应生成4mol Ag,说明分子中含有2个醛基;④苯环上的一卤代物只有一种,可能含有1个可被取代的H.
解答:
解:(1)设绿原酸的分子式为X,绿原酸与水按1:1发生反应,则有X+H2O→C7H12O6+C9H8O4,可知绿原酸的分子式为C16H18O9,反应①发生取代反应或水解反应,
故答案为:C16H18O9;取代反应;
(2)化合物I含有4个-OH和1个-COOH,都可与钠反应生成氢气,1mol化合物I与足量金属钠反应,可生成2.5mol氢气,在标准状况下的体积为2.5mol×22.4L/mol=56L,
故答案为:56 L;
(3)化合物II含有酚羟基,可与浓溴水发生取代反应,含有碳碳双键,可与溴水发生加成反应,反应的方程式为 ,
,
故答案为: ;
;
(4)对比化合物II和化合物Ⅲ,可知化合物II应和酸性比-COOH弱,但比酚羟基强的酸对应的盐反应,则只能为NaHCO3溶液,故答案为:NaHCO3溶液;
(5)①与化合物II互为同分异构体;②遇FeCl3溶液显色,说明分子中含有酚羟基;③1mol 化合物Ⅳ与足量银氨溶液反应生成4mol Ag,说明分子中含有2个醛基;④苯环上的一卤代物只有一种,可能含有1个可被取代的H,则可能的结构为 ,故答案为:
,故答案为: .
.
故答案为:C16H18O9;取代反应;
(2)化合物I含有4个-OH和1个-COOH,都可与钠反应生成氢气,1mol化合物I与足量金属钠反应,可生成2.5mol氢气,在标准状况下的体积为2.5mol×22.4L/mol=56L,
故答案为:56 L;
(3)化合物II含有酚羟基,可与浓溴水发生取代反应,含有碳碳双键,可与溴水发生加成反应,反应的方程式为
 ,
,故答案为:
 ;
;(4)对比化合物II和化合物Ⅲ,可知化合物II应和酸性比-COOH弱,但比酚羟基强的酸对应的盐反应,则只能为NaHCO3溶液,故答案为:NaHCO3溶液;
(5)①与化合物II互为同分异构体;②遇FeCl3溶液显色,说明分子中含有酚羟基;③1mol 化合物Ⅳ与足量银氨溶液反应生成4mol Ag,说明分子中含有2个醛基;④苯环上的一卤代物只有一种,可能含有1个可被取代的H,则可能的结构为
 ,故答案为:
,故答案为: .
.
点评:本题考查有机物的推断,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol H2O的质量为18g/mol |
| B、CH4的摩尔质量为16g |
| C、2.3克金属钠变为钠离子时失去的电子数是0.1NA |
| D、22.4 L SO2所含的分子数为NA |
下列溶液中除存在水分子外,还存在其它分子的是( )
| A、稀硫酸溶液 |
| B、氢氧化钠溶液 |
| C、醋酸溶液 |
| D、氯化钠溶液 |
当光束通过下列分散系时,能产生丁达尔效应的是( )
| A、NaCl溶液 |
| B、Fe(OH)3胶体 |
| C、盐酸 |
| D、硫酸铜溶液 |
下列说法正确的是( )
| A、强电解质溶液的导电能力一定比弱电解质溶液强 |
| B、中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多 |
| C、如果盐酸的浓度是醋酸的两倍,则盐酸的H+浓度也是醋酸的二倍 |
| D、物质的量相同的磷酸钠溶液和磷酸溶液中所含的PO43-不同 |
下列说法正确的是( )
| A、常温常压下,20g2H216O所含中子数为12 NA(NA表示阿伏加德罗常数的值,下同) |
| B、其他条件相同时,金属接触的电解质溶液的导电能力越强,其电化学腐蚀越快 |
| C、Na+、NO3-、Br-、OH-在遇K3Fe(CN)6产生蓝色沉淀的溶液中一定能大量共存 |
| D、1 mol FeCl3完全转化为Fe(OH)3胶体后生成NA个胶粒 |
能在透明溶液中大量共存的一组离子是( )
| A、Na+、NH4+、OH-、HCO3- |
| B、Mg2+、Ag+、NO3-、SiO32- |
| C、K+、Cu2+、Cl-、SO42- |
| D、H+、Fe3+、I-、ClO- |
已知0.02mol?L-1 CH3COOH溶液和0.01mol?L-1 NaOH溶液以等体积混和后溶液呈酸性,则该混合液中微粒浓度关系正确的( )
| A、c(CH3COO-)>c (Na+) |
| B、c(Na+)+c(H+)=c(OH-)+c(CH3COOH)+c(CH3COO-) |
| C、c(CH3COOH)>c(CH3COO-) |
| D、c(CH3COOH)+c(CH3COO-)=0.02mol?L-1 |
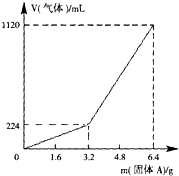 将一定量混合均匀的铁粉与硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A.将质量为m的固体A加入到300mL 2mol?L-1盐酸中使之完全溶解.测得室温下加入固体A的质量与收集到气体体积(已换算成标准状况)的关系如图15所示(假设所得氢硫酸溶液饱和前无硫化氢气体逸出).
将一定量混合均匀的铁粉与硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A.将质量为m的固体A加入到300mL 2mol?L-1盐酸中使之完全溶解.测得室温下加入固体A的质量与收集到气体体积(已换算成标准状况)的关系如图15所示(假设所得氢硫酸溶液饱和前无硫化氢气体逸出).