题目内容
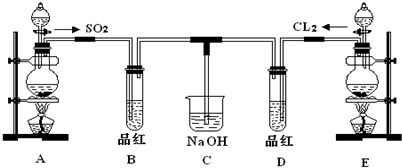
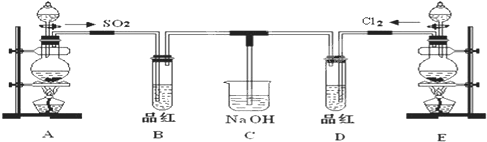
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置.
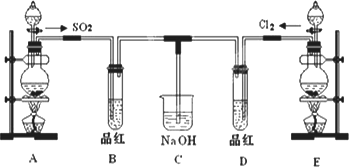
(1)实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:________;
(2)实验室用装置E制备Cl2,其反应的化学化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O.若有6 mol的HCl参加反应,则转移的电子总数为________;
MnCl2+Cl2↑+2H2O.若有6 mol的HCl参加反应,则转移的电子总数为________;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:________,D:________.
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:________,D:________.
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样.请你分析该现象的原因(用化学方程式表示)提示SO2有较强的还原性.
_________________________
答案:
解析:
解析:
|
(1)分液漏斗的玻璃塞没有取下来; (2)3×6.02×1023;或3NA (3)①品红褪色;品红褪色. ②褪色的品红又恢复成红色;无明显现象. (4)Cl2+SO2+2H2O |

练习册系列答案
相关题目
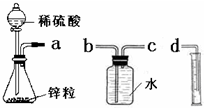 某化学实验小组的同学用下列仪器组装两套完全相同的装置定量探究浓度对反应速率的影响.
某化学实验小组的同学用下列仪器组装两套完全相同的装置定量探究浓度对反应速率的影响.(1)为达到本实验目的其装置连接顺序为:
a连
(2)连接好装置后的下一步操作是
(3)锥形瓶中发生反应的离子方程式为
(4)两套装置的分液漏斗所装的试剂分别为1mol/L硫酸和4mol/L硫酸,该小组同学要测定并记录的数据如下表:
| 加入的试剂 | H2的体积(相同条件下) | 反应时间 | 反应速率 |
| 1mol/L硫酸 | 10mL | t1 | v1 |
| 4mol/L硫酸 | 10mL | t2 | v2 |
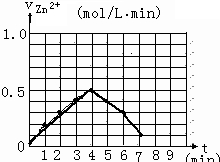
(5)另有一组同学测定了每隔一分钟,锥形瓶中硫酸的浓度,记录结果如下:
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 硫酸浓度(mol/L | 4.0 | 3.8 | 3.5 | 3.1 | 2.6 | 2.2 | 1.9 | 1.8 | … |
请解释0到4mim时该化学反应速率随时间变化的原因:
(6)除上述实验方案可定量测定该反应的化学反应速率外,还可能有的实验测定方案有: