题目内容
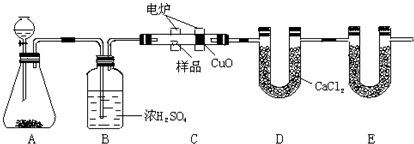
化学上常用燃烧法确定有机物的组成,如下图所示装置是用燃烧法确定烃或烃的含氧衍生物分子式的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成。
完成下列问题:
(1)A中发生反应的化学方程式为_______________________________________。
(2)B装置的作用是_______________________________________________,燃烧管C中CuO的作用是______________________________________________________。
(3)产生氧气按从左向右流向,燃烧管C与装置D、E的连接顺序是:C→________→__________。
(4)反应结束后,从A装置锥形瓶内的剩余物质中分离出固体,需要进行的实验操作是____________________________________________________________________。
(5)准确称取
解析:根据实验目的,是用燃烧法来测定有机物分子式的实验,通过测定H2O和CO2的质量从而求出有机物的组成或分子式。首先应明确各装置的作用,A装置是产生O2的装置,根据该装置的特点,属于“固+液”反应型,为此可用H2O2在MnO2催化下制得O2,或用Na2O2与H2O反应制得O2;装置B的作用是干燥O2;对于装置D、E的连接顺序首先用E中的CaCl2吸收H2O,再用D中的碱石灰吸收CO2,二者不能颠倒,因碱石灰既能吸收H2O,也能吸收CO2。样品在C中燃烧时,有可能燃烧不充分从而产生CO,通过CuO将CO完全转化为CO2,从而保证实验的准确性。D管增加的质量为CO2,即m(CO2)= 。
。
答案:(1)2H2O2![]() 2H2O+O2↑(或2Na2O2+2H2O
2H2O+O2↑(或2Na2O2+2H2O![]() 4NaOH+O2↑)
4NaOH+O2↑)
(2)吸收氧气中的水蒸气(或答:干燥氧气) 使有机物不完全燃烧的产物全部转化为CO2和H2O
(3)E D
(4)过滤〔蒸发结晶(需与Na2O2跟H2O反应制O2相对应)〕
(5)CH2O C3H6O3 HOCH2CH2COOH、![]()