题目内容
化学上常用燃烧法确定有机物的组成.下图装置是用燃烧法确定有机物化学式常用的装置,这种方法是在电炉加热时用纯氧氧化管内样品.根据产物的质量确定有机物的组成.
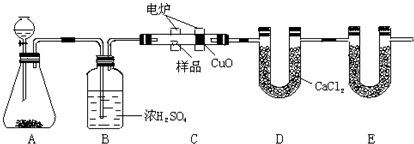
回答下列问题:
(1)A装置中分液漏斗盛放的物质是
(2)C装置(燃烧管)中CuO的作用是
(3)写出E装置中所盛放物质的名称
(4)若准确称取1.20g样品(只含C、H、O三种元素中的两种或三种).经充分燃烧后,E管质量增加1.76g,D管质量增加0.72g,则该有机物的最简式为

回答下列问题:
(1)A装置中分液漏斗盛放的物质是
H2O2(或双氧水)
H2O2(或双氧水)
,写出有关反应的化学方程式:2H2O2
2H2O+O2↑
| MnO2 |
2H2O2
2H2O+O2↑
.| MnO2 |
(2)C装置(燃烧管)中CuO的作用是
使有机物充分氧化生成CO2和H2O
使有机物充分氧化生成CO2和H2O
.(3)写出E装置中所盛放物质的名称
碱石灰或氢氧化钠
碱石灰或氢氧化钠
,它的作用是吸收CO2气体
吸收CO2气体
.(4)若准确称取1.20g样品(只含C、H、O三种元素中的两种或三种).经充分燃烧后,E管质量增加1.76g,D管质量增加0.72g,则该有机物的最简式为
CH2O
CH2O
.分析:明确各装置的作用是解题的前提,A用来制取反应所需的氧气、B用来吸收水、C是在电炉加热时用纯氧气氧化管内样品、D用来吸收产生的水、E是防止空气中的水进入D;根据一氧化碳能与氧化铜反应,可被氧化成二氧化碳的性质可知CuO的作用是把有机物不完全燃烧产生的CO转化为CO2;确定物质的化学式可借助元素的质量守恒进行解答.
解答:解:(1)双氧水可分解生成氧气,A装置中分液漏斗盛放的物质是双氧水,化学方程式:2H2O2
2H2O+O2↑
(2)CuO的作用是使有机物充分氧化生成CO2和H2O.
(3)E装置中所盛放物质最好选用碱石灰或氢氧化钠,因为氢氧化钠可以完全吸收反应生成的二氧化碳.故填碱石灰或氢氧化钠.它的作用是吸收CO2气体.
(4)本实验需测定有机物中碳元素、氢元素的质量,原理是根据氢氧化钠吸收的二氧化碳的质量求碳元素的质量,有机物燃烧时可能也产生一氧化碳,为了测定精确,要将有机物不完全燃烧产生的少量CO氧化成CO2,氧化铜通过与一氧化碳反应能保证有机物中的碳都转化为CO2;根据硫酸铜吸收的水的质量求氢元素的质量,然后根据碳、氢元素的质量和是否等于1.2克确定是否含有氧元素.过程如下:
E管质量增加1.76克说明生成了1.76克二氧化碳,可得碳元素的质量:1.76g×
×100%=0.48g
D管质量增加0.72克说明生成了0.72克水,可得氢元素的质量:0.72g×
×100%=0.08g
从而可推出含氧元素的质量为:1.2-0.48-0.08=0.64g
设最简式为CXHYOZ
12X:Y:16Z=0.48::0.08:0.64
X:Y:Z=1:2:1
最简式为 CH2O.
故答案为:(1)H2O2(或双氧水);2H2O
2H2O+O2↑;
(2)使有机物充分氧化生成CO2和H2O;
(3)碱石灰或氢氧化钠;吸收CO2气体;
(4)CH2O.
| MnO2 |
(2)CuO的作用是使有机物充分氧化生成CO2和H2O.
(3)E装置中所盛放物质最好选用碱石灰或氢氧化钠,因为氢氧化钠可以完全吸收反应生成的二氧化碳.故填碱石灰或氢氧化钠.它的作用是吸收CO2气体.
(4)本实验需测定有机物中碳元素、氢元素的质量,原理是根据氢氧化钠吸收的二氧化碳的质量求碳元素的质量,有机物燃烧时可能也产生一氧化碳,为了测定精确,要将有机物不完全燃烧产生的少量CO氧化成CO2,氧化铜通过与一氧化碳反应能保证有机物中的碳都转化为CO2;根据硫酸铜吸收的水的质量求氢元素的质量,然后根据碳、氢元素的质量和是否等于1.2克确定是否含有氧元素.过程如下:
E管质量增加1.76克说明生成了1.76克二氧化碳,可得碳元素的质量:1.76g×
| 12 |
| 44 |
D管质量增加0.72克说明生成了0.72克水,可得氢元素的质量:0.72g×
| 2 |
| 18 |
从而可推出含氧元素的质量为:1.2-0.48-0.08=0.64g
设最简式为CXHYOZ
12X:Y:16Z=0.48::0.08:0.64
X:Y:Z=1:2:1
最简式为 CH2O.
故答案为:(1)H2O2(或双氧水);2H2O
| MnO2 |
(2)使有机物充分氧化生成CO2和H2O;
(3)碱石灰或氢氧化钠;吸收CO2气体;
(4)CH2O.
点评:本题是一道较综合的实验题,主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目


