题目内容
1.某有机化合物结构简式为
a.写出其分子式C16H16O5.
b.分子中有2种双键.
分析 a、分子式是表示物质的元素组成的式子;
b、双键分为碳碳双键、碳氧双键和碳氮双键等.
解答 解:a、分子式是表示物质的元素组成的式子,此有机物中含16个C原子、16个H原子和2个氧原子,故分子式为C16H16O5,故答案为:C16H16O5;
b、双键分为碳碳双键、碳氧双键和碳氮双键等,此有机物中含碳碳双键和碳氧双键,故含有的双键有2种,故答案为:2.
点评 本题考查了有机物的分子式和官能团的结构,应注意的是碳碳双键有碳碳双键、碳氧双键等,难度不大.

练习册系列答案
相关题目
12.下列元素中,原子半径最大的是( )
| A. | 锂 | B. | 钠 | C. | 氟 | D. | 氯 |
9.与CO32-不是等电子体的是( )
| A. | SO3 | B. | BF3 | C. | NO3- | D. | PCl3 |
16.下列叙述能证明金属A的金属性比金属B强的是( )
| A. | A原子的最外层电子数比B原子最外层电子数少 | |
| B. | 常温下,A能从冷水中置换出氢气,而B不能 | |
| C. | 等物质的量A和B与足量稀硫酸反应,产生氢气的量A比B多 | |
| D. | A原子的电子层数比B原子电子层数多 |
6.X、Y、Z是原子序数依次增大的短周期主族元素,X2-、Z+都与Mg2+具有相同的核外电子层结构,下列说法中正确的是( )
| A. | Y元素位于第二周期第ⅦA族或0族 | |
| B. | X、Y、Z三种元素中非金属性最强的是X元素 | |
| C. | Y的最高氧化物对应的水化物是已知酸中最强的酸 | |
| D. | Z分别与X、Y形成的化合物都是离子化合物 |
13.下列有关物质的表达式正确的是( )
| A. | 乙烯的结构简式:CH2 CH2 | B. | 丙烯的球棍模型: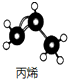 | ||
| C. | 醛基的结构简式:-COH | D. | 羟基的电子式: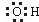 |
10.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 强酸性溶液:Mg2+、K+、SO42-、NO3- | |
| B. | 使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3- | |
| C. | 0.1mol•L-1AgNO3溶液:H+、K+、SO42-、I- | |
| D. | 0.1mol•L-lNaAlO2溶液:H+、Na+、Cl-、SO42- |
11.下列化学反应的离子方程式正确的是( )
| A. | 往NaOH溶液中通入过量SO2:SO2+2OH-═SO32-+H2O | |
| B. | 锌与稀硝酸反应:Zn+2H+═Zn2++H2↑ | |
| C. | 向氯化铵的溶液中加入足量浓KOH溶液并加热:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3•H2O | |
| D. | 向氯水中通入SO2气体:Cl2+SO2+2H2O═4H++2Cl-+SO42- |
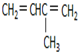 2-甲基-1,3-丁二烯;
2-甲基-1,3-丁二烯;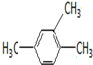 1,2,4-三甲基苯;
1,2,4-三甲基苯;