题目内容
16.下列叙述能证明金属A的金属性比金属B强的是( )| A. | A原子的最外层电子数比B原子最外层电子数少 | |
| B. | 常温下,A能从冷水中置换出氢气,而B不能 | |
| C. | 等物质的量A和B与足量稀硫酸反应,产生氢气的量A比B多 | |
| D. | A原子的电子层数比B原子电子层数多 |
分析 判断金属性强弱的依据:元素原子的失电子能力、单质从酸(或水)中置换的H2的难易程度等.
解答 解:A、金属性强弱和原子的最外层电子数无关,如氢原子最外层只有一个电子,而镁原子最外层两个电子,镁的金属性更强,故A错误;
B、常温时,A能从冷水中置换出氢气而B不能与冷水反应,说明A的金属性比B强,故B正确;
C、金属性强弱取决于单质从酸(或水)中置换的H2的难易程度,和置换的H2多少无关,故C错误;
D、金属性强弱和原子的电子层数多少无关,如氢原子只有一个电子层,而镁原子有三个电子层,镁的金属性更强,故D错误.
故选B.
点评 本题考查学生判断金属性强弱的依据,学生要清楚金属性的强弱与失电子的难易有关而跟失电子的多少无关,难度不大.

练习册系列答案
相关题目
7.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一种反应物”在40℃~50℃时反应可生成它.CuH不稳定、易分解,CuH在氯气中能燃烧,跟盐酸反应能产生气体,以下有关它的推断中错误的是( )
| A. | “另一种反应物”一定具有还原性 | B. | “另一种反应物”一定只具有氧化性 | ||
| C. | 2CuH+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl | D. | CuH既可作氧化剂也可作还原剂 |
4.已知元素X、Y同周期,且电负性X>Y,下列说法错误的是( )
| A. | X的原子序数一定大于Y | |
| B. | 第一电离能Y一定小于X | |
| C. | X和Y在形成化合物时,X显负价、Y显正价 | |
| D. | 气态氢化物的稳定性:HmX强于HnY |
11.具有下列电子排布式的原子中,半径最大的是( )
| A. | ls22s22p63s23p5 | B. | 1s22s22p3 | C. | 1s22s22sp5 | D. | 1s22s22p63s23p4 |
8.X、Y、Z、W、R五种短周期元素原子序数依次增大,X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料,下列相关说法正确的是( )
| A. | W的最高价氧化物对应的水化物难溶于水 | |
| B. | 原子半径按X、Y、Z、R、W的顺序依次增大 | |
| C. | Z与Y形成的化合物是碱性氧化物 | |
| D. | WY2能与强碱溶液反应,但不能与任何酸反应 |
5.下列叙述正确的是( )
| A. | 金属元素和非金属元素形成的化合物一定是离子化合物 | |
| B. | 18O2和18O3互为同素异形体,相同状况下其密度之比为2:3 | |
| C. | 过渡元素都是副族元素 | |
| D. | 同主族元素的原子最外层电子数相同,化学性质也相同 |
6.水溶液中能大量共存的一组离子是( )
| A. | Na+、Ba2+、Cl-、SO42- | B. | Fe2+、H+、S2-、ClO- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、OH-、NO3-、HSO3- |
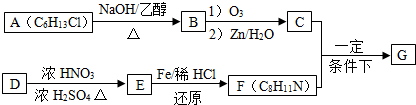
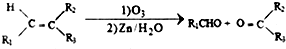

 .
.

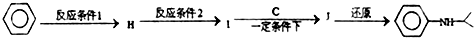
 .
.