题目内容
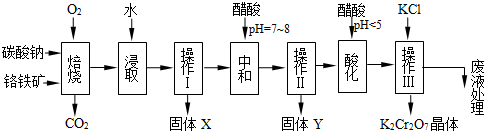
重铬酸钾(K2Cr2O7)是橙色晶体,铬酸钾(K2CrO4)是黄色晶体,将重铬酸 钾溶于水配成2%的溶液,重铬酸钾发生水解,反应的离子方程式为H2O+Cr2O72- =2CrO42-+2H+,当达到平衡时,溶液颜色介于橙色和黄色之间。
(1)当滴入10滴2mol·L-1NaOH溶液于3mL2%K2Cr2O7溶液中,溶液变________ 色,理由________(2)将5滴2mol·L-1的H2SO4溶液加入上述(1)所得溶液中,现象________,理由 ________(3)在上述(2)所得溶液中,再滴入5滴2mol·L-1H2SO4溶液,现象________,理 由是________
答案:
解析:
解析:
(1) 黄 加入OH-使c(H+)降低,平衡右移,c(CrO (2)橙黄色 H2S04刚好中和所加NaOH,平衡基本恢复原状(3)橙色 c(H+)增大,平衡左移,c(Cr2O
|

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目