题目内容
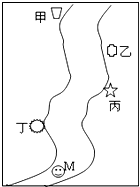 如图所示,在一条鱼、虾几乎绝迹的小河边,从上游到下游依次有甲、乙、丙、丁四座工厂,各厂排放的废水里都只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:①甲处河水呈乳白色;②乙处河水呈红褐色;③丙处河水由浑变清;④丁处产生气泡,河水仍澄清. 四座工厂排出的废水里含有的污染物分别为:
如图所示,在一条鱼、虾几乎绝迹的小河边,从上游到下游依次有甲、乙、丙、丁四座工厂,各厂排放的废水里都只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水监测时发现:①甲处河水呈乳白色;②乙处河水呈红褐色;③丙处河水由浑变清;④丁处产生气泡,河水仍澄清. 四座工厂排出的废水里含有的污染物分别为:甲
考点:几组未知物的检验
专题:物质检验鉴别题
分析:水流方向是由甲经过乙,依次流经丙和丁,根据四种物质的性质特点,甲处河水呈乳白色,故为Ca(OH)2;乙处河水呈红褐色是因为生成了Fe(OH)3,故乙处为FeCl3;丙处河水由浑变清,是由于Fe(OH)3沉淀在丙处被溶解,故丙处为盐酸,丁处为Na2CO3(与盐酸作用产生气泡).
解答:
解:水流方向是由甲经过乙,依次流经丙和丁,根据四种物质的性质特点,甲处河水呈乳白色,故为Ca(OH)2;乙处河水呈红褐色是因为生成了Fe(OH)3,故乙处为FeCl3;丙处河水由浑变清,是由于Fe(OH)3沉淀在丙处被溶解,故丙处为盐酸,丁处为Na2CO3(与盐酸作用产生气泡),
由上述分析可知,四座工厂排出的废水含有的污染物分别为:甲为Ca(OH)2;乙为FeCl3;丙为HCl;丁为Na2CO3;
故答案为:Ca(OH)2;FeCl3;HCl;Na2CO3.
由上述分析可知,四座工厂排出的废水含有的污染物分别为:甲为Ca(OH)2;乙为FeCl3;丙为HCl;丁为Na2CO3;
故答案为:Ca(OH)2;FeCl3;HCl;Na2CO3.
点评:本题以四种常见物质之间的离子反应为切入点,从环保的角度考查知识的实际应用,本题实质是框图型物质推断题,根据物质的溶解性,确定甲处废水含有Ca(OH)2,是推断的突破口,再结合物质间的反应判断.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、将73gHCl溶于水中配成1L溶液,所得溶液物质的量浓度是2mol/L |
| B、水的摩尔质量是18g |
| C、在标准状况下,1mol任何物质的体积都约为22.4L |
| D、标准状况下,1.8L H2O和1.8L NH3所含分子个数相同 |
下列说法正确的是( )
| A、SO2、SiO2、NO2均为酸性氧化物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、二氧化碳、冰醋酸、四氯化碳均为非电解质 |
| D、福尔马林、水玻璃、氨水均为混合物 |
某无色溶液可能含有AgNO3、NaCl、Na2CO3和Na2SO4中的一种.取少量该溶液于试管中,加入稀盐酸,无明显现象,再加入BaCl2溶液,有白色沉淀产生.则该物质是( )
| A、AgNO3 |
| B、NaCl |
| C、Na2CO3 |
| D、Na2SO4 |
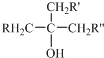 中的-OH不能被氧化.
中的-OH不能被氧化.