题目内容
19.在一定温度和压强下,气体体积主要取决于( )| A. | 气体分子数目的多少 | B. | 气体分子微粒大小 | ||
| C. | 气体分子间的平均距离 | D. | 气体分子量的大小 |
分析 在一定温度和压强下,气体分子间距离一定,影响气体体积的因素有分子间距离和分子数目,在相同条件下,气体的分子间距离相等,以此分析.
解答 解:A.在一定温度和压强下,气体分子间距离一定,气体分子微粒大小与分子间距离相比较可忽略不计,所以影响气体大小的因素主要取决于气体分子数目的多少,故A正确;
B.气体分子微粒大小与分子间距离相比较可忽略不计,不是影响气体体积大小的因素,故B错误;
C.在一定温度和压强下,气体分子间距离一定,不是影响气体体积大小的因素,故C错误;
D.气体分子的相对分子质量与气体的体积无关,故D错误.
故选A.
点评 本题考查影响气体体积的因素,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
9.25℃时,5种银盐的溶度积常数(Ksp)分别是:
下列说法正确的是( )
| AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
| A. | 氯化银、溴化银和碘化银的溶解度依次增大 | |
| B. | 将硫酸银溶解于水后,向其中加入少量硫化钠固体,不能得到黑色沉淀 | |
| C. | 在5mL1.5×10-5 mol•L-1的NaCl溶液中,加入1滴(1mL约20滴)1.0×10-3mol•L-1的AgNO3溶液,不能观察到白色沉淀 | |
| D. | 在烧杯中放入6.24 g 硫酸银固体,加200 g 水,经充分溶解后,所得饱和溶液的体积为200 mL,溶液中Ag+ 的物质的量浓度为0.2 mol•L-1 |
10. 合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.
合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.
(一)煤化工生产中生产合成气的反应为:C(s)+H20(g)?C0(g)+H2(g)△H1
已知:C(s)+$\frac{1}{2}$O2(g)=C0(g)△H2=-110.5kJ•mol-1
H2(g)+$\frac{1}{2}$02(g)=H20(g)△H3=-242kJ•mol-1
(1 )反应C(s)+H20(g)?C0(g)+H2(g)在高温(填高温或低温)下自发进行,理由是△H1=△H2-△H3=131.5kJ>0,△S>0.
(2)在恒温恒容下,同时放入C(s)、H20(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H20(g)?C0(g)+H2(g))已达到平衡的是ACD.
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH-0键断裂的同时有1molH-H键断裂
D.混合气体的平均相对分子质量为18且保持不变
(二)天然气化工中生产合成气的主要反应为:
2CH4(g)+02(g)?2C0(g)+4H2(g)△H=-23kJ•mol-1
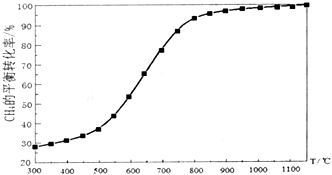
在恒容容器中按物质的量之比1:2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
(3)图中所表示的CH4的平衡转化率随温度变化的曲线,实质上是多个反应共同作用的结果.与之相关的反应还有以下三个反应:
I.CH4(g)+2O2(g)?C02(g)+2H20(g)△H5=-802kJ•mol-1
Ⅱ.CH4(g)+H2O(g)?C0(g)+3H2(g)△H6=+201kJ•mol-1
Ⅲ.CO(g)+H2O(g)?CO2(g)+H2(g)△H7=-35kJ•mol-1
你认为上述反应中,在高温下占主导地位的是Ⅱ(填反应序号).
(4)根据平衡移动原理,请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线.
(5)工业上常用选择性来判断不同反应条件下目标产物的产率,即:选择性=$\frac{目标产物的产率}{反应原料的转化率}$,现有实验测得反应2CH4(g)+02(g)?2CO(g)+4H2(g)在750℃下,以不同碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示:
最佳碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]为1:0.5.假设按碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]=l:1投料,反应容器的体积为VL,通入CH4和02各amol,请列式表示平衡时容器内C0的浓度(用a、V的代数式表示)$\frac{a×0.98×0.65}{V}$mol/L.
 合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.
合成气(C0+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品.(一)煤化工生产中生产合成气的反应为:C(s)+H20(g)?C0(g)+H2(g)△H1
已知:C(s)+$\frac{1}{2}$O2(g)=C0(g)△H2=-110.5kJ•mol-1
H2(g)+$\frac{1}{2}$02(g)=H20(g)△H3=-242kJ•mol-1
(1 )反应C(s)+H20(g)?C0(g)+H2(g)在高温(填高温或低温)下自发进行,理由是△H1=△H2-△H3=131.5kJ>0,△S>0.
(2)在恒温恒容下,同时放入C(s)、H20(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H20(g)?C0(g)+H2(g))已达到平衡的是ACD.
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH-0键断裂的同时有1molH-H键断裂
D.混合气体的平均相对分子质量为18且保持不变
(二)天然气化工中生产合成气的主要反应为:
2CH4(g)+02(g)?2C0(g)+4H2(g)△H=-23kJ•mol-1
在恒容容器中按物质的量之比1:2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
(3)图中所表示的CH4的平衡转化率随温度变化的曲线,实质上是多个反应共同作用的结果.与之相关的反应还有以下三个反应:
I.CH4(g)+2O2(g)?C02(g)+2H20(g)△H5=-802kJ•mol-1
Ⅱ.CH4(g)+H2O(g)?C0(g)+3H2(g)△H6=+201kJ•mol-1
Ⅲ.CO(g)+H2O(g)?CO2(g)+H2(g)△H7=-35kJ•mol-1
你认为上述反应中,在高温下占主导地位的是Ⅱ(填反应序号).
(4)根据平衡移动原理,请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线.
(5)工业上常用选择性来判断不同反应条件下目标产物的产率,即:选择性=$\frac{目标产物的产率}{反应原料的转化率}$,现有实验测得反应2CH4(g)+02(g)?2CO(g)+4H2(g)在750℃下,以不同碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示:
| 碳氧比[$\frac{n(C{H}_{4})}{n({O}_{2})}$] | 1:0.25 | 1:0.5 | 1:1 | 1:1.25 |
| CH4转化率 | 0.40 | 0.88 | 0.98 | 0.99 |
| H2选择性 | 0.98 | 0.93 | 0.67 | 0.40 |
| CO选择性 | 0.99 | 0.94 | 0.65 | 0.32 |
7.已知A(g)+B(g)?C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1.,则6s时c(A)=0.022 mol•L-1,
n(C)=0.09mol;若反应经一段时间后,达到平衡后,如果这时再向该密闭容器中再充入1mol氩气,平衡时A的转化率α(A)=80%;
(3)判断该反应是否达到平衡的依据为c:
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的k=2.5.
| |温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1.,则6s时c(A)=0.022 mol•L-1,
n(C)=0.09mol;若反应经一段时间后,达到平衡后,如果这时再向该密闭容器中再充入1mol氩气,平衡时A的转化率α(A)=80%;
(3)判断该反应是否达到平衡的依据为c:
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的k=2.5.
14.已知KSP(Ag2CrO4)=1.12×10-12,将等体积的4×10-3mo1•L-1的AgNO3和4×10-3mo1•L-1K2CrO4混合,能产生Ag2CrO4沉淀(填“能”或“不能”).
4.对“AgCl(s)?Ag+(aq)+Cl-(aq)”的理解正确的是( )
①说明AgCl没有完全电离,AgCl是弱电解质
②说明溶解的AgCl已完全电离,是强电解质
③说明Cl-与Ag+的反应不能完全进行到底
④说明Cl-与Ag+的反应可以完全进行到底.
①说明AgCl没有完全电离,AgCl是弱电解质
②说明溶解的AgCl已完全电离,是强电解质
③说明Cl-与Ag+的反应不能完全进行到底
④说明Cl-与Ag+的反应可以完全进行到底.
| A. | ③④ | B. | ③ | C. | ①③ | D. | ②④ |
11.在温度、容积相同的 3 个密闭容器中,按不同方式 投入反应物,保持恒温、恒容,测 得反应达到平衡时的有关数据如表(已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1)
下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A. | α1+α3<1 | B. | a+b>92.4 | C. | 2p2<p3 | D. | 2c1>c3 |
9.常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )

| A. | 在任何溶液中,若有CaSO4沉淀析出,则c(Ca2+)与c(SO42-)一定相等 | |
| B. | d点溶液通过蒸发可以变到c点 | |
| C. | a点对应的Ksp等于c点对应的Ksp | |
| D. | b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3mol/L |