题目内容
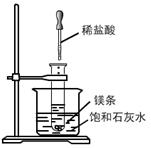
已知Ca(OH)2的溶解度随温度升高而降低。如下图所示, 在试管中放入少许镁条,将试管浸入盛饱和石灰水的烧杯中,再向试管中滴入5mL 5mol · L-1盐酸。

(1)实验中可观察到的现象有:
①_____________________ _ ______;
②_____________________________ _____。
(2)试管中发生反应的离子方程式为______________________________。
(3)由实验推知,镁条和盐酸的总能量_________(填“大于”、“小于”或“等于”)MgCl2 溶液和H2的总能量。判断的根据是__________ ___________。
(10分)
(1)①镁条上有气泡逸出 ②饱和石灰水变浑浊 (各2分,共4分)
(2)Mg+2H+=Mg2++H2↑ (2分)
(3)大于(2分);因为盐酸与Mg反应是放热反应,故反应物总能量应大于生成物总能量(2分)

 步步高达标卷系列答案
步步高达标卷系列答案某研究性学习小组对还原铁粉与水蒸气的反应产物进行科学探究。已知Ca(OH)2的分解温度为580℃,铁粉与水蒸气反应的温度为900℃:根据下图所示实验装置,进行了还原铁粉与水蒸气的反应实验,实验中观察到肥皂液中产生了大量的气泡。
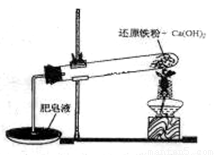
(1)实验中Ca(OH)2的作用是 。实验中产生的气体产物是 。
(2)为进一步探究还原铁粉与水蒸气反应固体产物的成分,研究性学习小组将反应后的固体经处理后得到黑色氧化物固体,针对黑色氧化物固体,该小组提出如下的假设并进行了相关的实验:
假设一:固体为FeO
假设二:固体为Fe3O4
假设三:
①限选用下列试剂:盐酸、KSCN溶液、K3Fe(CN)6 溶液、氯水,证明假设一不成立
|
操作 |
现象 |
结论 |
|
|
|
假设一不成立 |
②为了进一步确定产物的成分,用黑色固体进行了下列实验:

加入足量氯水所发生反应的离子方程式是 ;检验红褐色固体是否洗涤干净的操作是 ;灼烧时盛放固体的仪器是 ;若假设二成立,黑色固体最终全部转化成的红棕色粉末的质量是 g