题目内容
【题目】阿斯巴甜(Aspartame)是一种具有清爽甜味的有机化合物,结构简式如图所示。下列说法不正确的是

A. 阿斯巴甜属于氨基酸,分子式为C14H18N2O5
B. 阿斯巴甜分子的核磁共振氢谱共有11种吸收峰
C. 阿斯巴甜能发生氧化、取代、消去等反应
D. 阿斯巴甜在一定条件下既能与酸反应,又能与碱反应
【答案】C
【解析】该有机物结构中含有氨基和羧基,所以阿斯巴甜属于氨基酸,分子式为C14H18N2O5;A正确;该结构中以侧链取代基为对称轴,如图: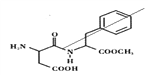 核磁共振氢谱共有11种吸收峰,B正确;该有机物能够燃烧,发生氧化反应,含有肽键,发生水解,没有醇羟基,不能发生消去反应,C错误;含-COOH和-NH2,阿斯巴甜在一定条件下既能与酸反应,又能与碱反应, D正确;正确选项C。
核磁共振氢谱共有11种吸收峰,B正确;该有机物能够燃烧,发生氧化反应,含有肽键,发生水解,没有醇羟基,不能发生消去反应,C错误;含-COOH和-NH2,阿斯巴甜在一定条件下既能与酸反应,又能与碱反应, D正确;正确选项C。

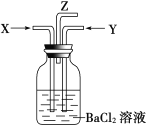
【题目】某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作如下: ①用标准溶液润洗滴定管2-3 次,取标准NaOH 溶液注入碱式滴定管至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“0”或“0”刻度线稍下,并记下读数;④量取20.00mL待测液注入清净的锥形瓶中,并加入3滴酚酞溶液;⑤用标准液滴定至终点,记下滴定管液面读数;⑥重复以上滴定操作2-3 次。
请回答下列问题:
(1)步骤④中,若在取盐酸的滴定管尖嘴部分有气泡且取液结束前气泡消失,则测定结果____(填“偏大”、“偏小”或“无景响”)。
(2)判断到达滴定路点的依据是____________。
(3)以下是实验数据记录表
滴定次数 | 盐酸体积(mL) | NaOH溶液体积读数(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.00 | 21.10 |
2 | 20.00 | 0.00 | 19.40 |
3 | 20.00 | 0.00 | 19.32 |
以上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是__________
A.NaOH 标准液保存时间过长,有部分变质
B.锥形瓶用待测液润洗
C.配制NaOH 标准液所用的药品中混有KOH固体
D.滴定结束时,俯视读数
(4)根据上表记录数据,通过计算可得,该盐酸浓度为_____mol/L。
(5)室温下,用0.100mol/LNaOH溶液分别滴定20.00mL0.100mol/L的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是_________
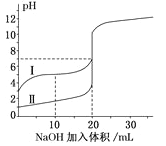
A.V(NaOH)=20mL时,c(Cl-)=c(CH3COO-)
B.I表示的是滴定盐酸的曲线
c.pH=7时,滴定醋酸消耗V(NaOH)小于20mL
D.V(NaOH)=10mL时,醋酸溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)