题目内容
下列各反应,能用同一离子方程式表示的是( )
| A、醋酸和氢氧化钠溶液 醋酸和氨水 |
| B、氯化钡溶液与硫酸铜溶液 氢氧化钡溶液与硫酸铜溶液 |
| C、氢氧化钡与稀硫酸 氢氧化钡与稀盐酸 |
| D、石灰石与稀硝酸 石灰石与稀盐酸 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧化钠是强电解质,一水合氨是弱电解质;
B.氯化钡和硫酸铜反应生成硫酸钡沉淀和可溶性的氯化铜,氢氧化钡和硫酸铜反应生成氢氧化铜和硫酸钡沉淀;
C.氢氧化钡和稀硫酸反应生成硫酸钡沉淀和水,氢氧化钡和稀盐酸反应生成氯化钡和水;
D.石灰石都是难溶物,稀硝酸和稀盐酸都是强酸.
B.氯化钡和硫酸铜反应生成硫酸钡沉淀和可溶性的氯化铜,氢氧化钡和硫酸铜反应生成氢氧化铜和硫酸钡沉淀;
C.氢氧化钡和稀硫酸反应生成硫酸钡沉淀和水,氢氧化钡和稀盐酸反应生成氯化钡和水;
D.石灰石都是难溶物,稀硝酸和稀盐酸都是强酸.
解答:
解:A.醋酸和氢氧化钠溶液离子方程式为CH3COOH+OH-=CH3COO-+H2O,醋酸和氨水混合反应离子方程式为CH3COOH+NH3.H2O=NH4++CH3COOH+H2O,所以二者离子方程式不同,故A错误;
B.氯化钡和硫酸铜反应生成硫酸钡沉淀和可溶性的氯化铜,离子反应方程式为Ba2++SO42-=BaSO4↓,氢氧化钡和硫酸铜反应生成氢氧化铜和硫酸钡沉淀,离子反应方程式为,Ba2++2OH-+SO42-+Cu2+=Cu(OH)2+BaSO4↓,所以二者不同,故B错误;
C.氢氧化钡和稀硫酸反应生成硫酸钡沉淀和水,离子方程式为Ba2++2OH-+SO42-+2H+=2H2O+BaSO4↓,氢氧化钡和稀盐酸反应生成氯化钡和水,离子方程式为OH-+H+=H2O,故C错误;
D.石灰石都是难溶物,稀硝酸和稀盐酸都是强酸,离子方程式都是CaCO3+2H+=Ca2++CO2↑+H2O,所以离子方程式相同,故D正确;
故选D.
B.氯化钡和硫酸铜反应生成硫酸钡沉淀和可溶性的氯化铜,离子反应方程式为Ba2++SO42-=BaSO4↓,氢氧化钡和硫酸铜反应生成氢氧化铜和硫酸钡沉淀,离子反应方程式为,Ba2++2OH-+SO42-+Cu2+=Cu(OH)2+BaSO4↓,所以二者不同,故B错误;
C.氢氧化钡和稀硫酸反应生成硫酸钡沉淀和水,离子方程式为Ba2++2OH-+SO42-+2H+=2H2O+BaSO4↓,氢氧化钡和稀盐酸反应生成氯化钡和水,离子方程式为OH-+H+=H2O,故C错误;
D.石灰石都是难溶物,稀硝酸和稀盐酸都是强酸,离子方程式都是CaCO3+2H+=Ca2++CO2↑+H2O,所以离子方程式相同,故D正确;
故选D.
点评:本题考查了离子方程式的书写,明确离子方程式的书写规则及发生的反应是解本题关键,易错选项是C.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| B、常温常压,64g SO2中含有的原子数为3NA |
| C、标准状况下,11.2L H2O含有的分子数为0.5NA |
| D、物质的量浓度为0.5 mol?L-1的MgCl2溶液,含有Cl-数目为 NA |
下列各组顺序的排列不正确的是( )
| A、非金属性:Si>C>P>Cl>F |
| B、热稳定性;HCl>H2S>PH3>AsH3 |
| C、酸性强弱:H3AlO3<H2SiO4<H2CO3<H3PO4 |
| D、离子半径;F->Na+>Mg2+>Al3+ |
下列叙述正确的是( )
| A、0.1 mol?L-1CH3COOH溶液加水稀释,溶液中所有离子浓度均减小 |
| B、常温下,在由水电离出的c(OH-)=1×10-12mol?L-1的溶液中,Al3+可能大量存在 |
| C、常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,Ksp(AgCl)增大 |
| D、常温下,相同浓度的CH3COONa溶液与Na2CO3溶液相比,Na2CO3溶液的pH小 |
在10L密闭容器中进行如下反应:A(g)+B(g)?2C(g),2分钟后,B由2mol减少到1.2mol,则用单位内A的浓度变化表示的反应速率(VA)是( )
| A、0.02mol/(L?min) |
| B、0.04mol/(L?min) |
| C、0.08mol/(L?min) |
| D、0.8mol/(L?min) |
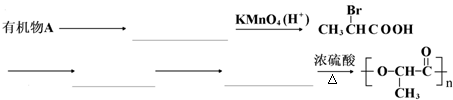
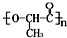 是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋.请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)
是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋.请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)