题目内容
硫、氮、稀土元素的单质和化合物应用广泛.
I.工业上可以通过将辉铜矿(Cu2S)在氧气中焙烧制备铜单质,该方法称为火法炼铜.化学方程式如下:
Cu2S+O2
2Cu+SO2
该过程中,铜元素被 (填“氧化”还是“还原”)成铜单质.制1molCu需转移 mol电子.
Ⅱ.①亚硝酸是一种不稳定的弱酸,但其盐的稳定性较好.亚硝酸铵水溶液呈酸性,请用合适的化学用语结合文字解释其原因: ;
②在亚硝酸铵溶液中所含离子浓度由大到小的顺序依次为 .
Ⅲ.稀土元素是宝贵的战略资源,铈(Ce)是地壳中含量最高的稀土元素.如图是其中一种提取铈的工艺流程:
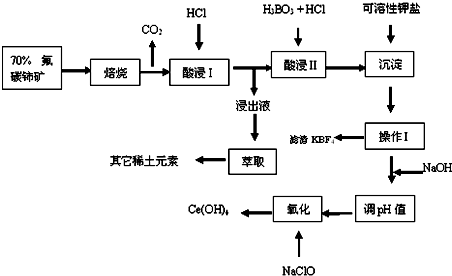
已知:i.焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;
ii.酸浸I的浸出液中含少量的+3价的铈.
①在生产过程中,酸浸I 中会产生黄绿色气体,污染环境、腐蚀设备.产生黄绿色气体的离子方程式是: ;若改成 ,就可以避免在该步骤中出现这个污染问题.
②在操作I后的溶液中加入NaOH溶液是为了调节溶液pH值获得Ce(OH)3,测定该溶液pH值的操作是
③写出流程中“氧化”步骤的化学反应方程式: .
I.工业上可以通过将辉铜矿(Cu2S)在氧气中焙烧制备铜单质,该方法称为火法炼铜.化学方程式如下:
Cu2S+O2
| ||
该过程中,铜元素被
Ⅱ.①亚硝酸是一种不稳定的弱酸,但其盐的稳定性较好.亚硝酸铵水溶液呈酸性,请用合适的化学用语结合文字解释其原因:
②在亚硝酸铵溶液中所含离子浓度由大到小的顺序依次为
Ⅲ.稀土元素是宝贵的战略资源,铈(Ce)是地壳中含量最高的稀土元素.如图是其中一种提取铈的工艺流程:

已知:i.焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;
ii.酸浸I的浸出液中含少量的+3价的铈.
①在生产过程中,酸浸I 中会产生黄绿色气体,污染环境、腐蚀设备.产生黄绿色气体的离子方程式是:
②在操作I后的溶液中加入NaOH溶液是为了调节溶液pH值获得Ce(OH)3,测定该溶液pH值的操作是
③写出流程中“氧化”步骤的化学反应方程式:
考点:铜金属及其重要化合物的主要性质,金属的回收与环境、资源保护
专题:实验设计题,元素及其化合物
分析:Ⅰ.标注元素化合价变化,依据氧化还原反应的概念分析判断,还原剂被氧化生成氧化产物,氧化剂被还原生成氧化产物,然后根据化合价的变化来确定移转电子的物质的量;
Ⅱ.①在亚硝酸铵溶液中,两种弱离子都水解,铵根离子水解程度大于亚硝根离子,亚硝酸铵水溶液呈酸性;
②在亚硝酸铵溶液中,水解程度小的最大,水解程度大的第二,显性的第三,最小的是隐性的;
Ⅲ①在生产过程中,酸浸I中会产生大量黄绿色气体,说明Ce4+离子具有强氧化性,可将Cl-氧化为Cl2,酸不能是氧化性的酸,也不能是盐酸;
②实验室测定PH的方法是撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
③由题目中“酸浸I的浸出液中含少量的+3价的铈”可知,加入NaOH后生成Ce(OH)3,NaClO将Ce(OH)3氧化为Ce(OH)4.
Ⅱ.①在亚硝酸铵溶液中,两种弱离子都水解,铵根离子水解程度大于亚硝根离子,亚硝酸铵水溶液呈酸性;
②在亚硝酸铵溶液中,水解程度小的最大,水解程度大的第二,显性的第三,最小的是隐性的;
Ⅲ①在生产过程中,酸浸I中会产生大量黄绿色气体,说明Ce4+离子具有强氧化性,可将Cl-氧化为Cl2,酸不能是氧化性的酸,也不能是盐酸;
②实验室测定PH的方法是撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
③由题目中“酸浸I的浸出液中含少量的+3价的铈”可知,加入NaOH后生成Ce(OH)3,NaClO将Ce(OH)3氧化为Ce(OH)4.
解答:
解:Ⅰ.Cu2S+O2=2Cu+SO2,铜元素化合价从+1价降到0价,被还原,氧元素化合价从 0价降低到-2价,硫元素化合价从-2价升高到+4价,消耗1molCu2S,电子转移6mol,生成1mol的铜转移3mol的电子,故答案为:还原,3;
II.①在亚硝酸铵溶液中,亚硝酸根和铵根分别可以发生水解反应:NO2-+H2O?HNO2+OH- 和 NH4++H2O?NH3?H2O+H+,由于铵根的水解程度大于亚硝酸根的水解,所以溶液呈酸性,
故答案为:亚硝酸根和铵根分别可以发生水解反应:NO2-+H2O?HNO2+OH- 和 NH4++H2O?NH3?H2O+H+,由于铵根的水解程度大于亚硝酸根的水解,所以溶液呈酸性;
②在亚硝酸铵溶液中,水解程度小的最大,水解程度大的第二,显性的第三,最小的是隐性的,所以c(NO2-)>c(NH4+ )>c(H+)>c(OH-),
故答案为:(NO2-)>c(NH4+ )>c(H+)>c(OH-);
Ⅲ①在生产过程中,酸浸I中会产生大量黄绿色气体,说明Ce4+离子具有强氧化性,可将Cl-氧化为Cl2,为避免污染环境、腐蚀设备,应用硫酸酸浸,
故答案为:2Ce4++2Cl-=2Ce3++Cl2↑;用H2SO4酸浸;
②实验室测定PH的方法是撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
故答案为:撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
③NaClO将Ce(OH)3氧化为Ce(OH)4,其中NaCl为还原产物,方程式为2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl,
故答案为:2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl.
II.①在亚硝酸铵溶液中,亚硝酸根和铵根分别可以发生水解反应:NO2-+H2O?HNO2+OH- 和 NH4++H2O?NH3?H2O+H+,由于铵根的水解程度大于亚硝酸根的水解,所以溶液呈酸性,
故答案为:亚硝酸根和铵根分别可以发生水解反应:NO2-+H2O?HNO2+OH- 和 NH4++H2O?NH3?H2O+H+,由于铵根的水解程度大于亚硝酸根的水解,所以溶液呈酸性;
②在亚硝酸铵溶液中,水解程度小的最大,水解程度大的第二,显性的第三,最小的是隐性的,所以c(NO2-)>c(NH4+ )>c(H+)>c(OH-),
故答案为:(NO2-)>c(NH4+ )>c(H+)>c(OH-);
Ⅲ①在生产过程中,酸浸I中会产生大量黄绿色气体,说明Ce4+离子具有强氧化性,可将Cl-氧化为Cl2,为避免污染环境、腐蚀设备,应用硫酸酸浸,
故答案为:2Ce4++2Cl-=2Ce3++Cl2↑;用H2SO4酸浸;
②实验室测定PH的方法是撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
故答案为:撕下一小片pH试纸放在干燥洁净的表面皿上,用玻璃棒蘸取该溶液点在pH试纸的中央,然后与标准比色卡对比;
③NaClO将Ce(OH)3氧化为Ce(OH)4,其中NaCl为还原产物,方程式为2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl,
故答案为:2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl.
点评:本题既有常规知识的考查又有新情景题目的考查,常规题目涉及到氧化还原、盐的水解和离子浓度大小比较;命题情景要求根据题意写出有关反应的方程式,做题时注意根据物质的性质正确判断反应物和生成物,用守恒的方法去书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
当0.2molNa2O2足量CO2完全反应后所得固体的质量为( )
| A、21.2g |
| B、21.6g |
| C、22.0g |
| D、22.4g |
下列分子中,各原子处于同一平面的是( )
| A、CH2O |
| B、NH3 |
| C、CCl4 |
| D、PCl3 |
下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不正确的是( )
A、淀粉
| ||||
B、纤维素
| ||||
C、油脂
| ||||
D、蛋白质
|
地壳中含量第一和第二的两种元素所形成的化合物不具有的性质是( )
| A、熔点很高 |
| B、与水反应生成对应的酸 |
| C、可与烧碱反应生成盐 |
| D、坚硬 |
电解质和非电解质是对化合物的一种分类方式.下列关于电解质的说法正确的是( )
| A、液态HCl不导电,所以HCl不是电解质 |
| B、NH3溶于水形成的溶液能导电,所以NH3是电解质 |
| C、电解质一定能导电,能导电的物质一定属于电解质 |
| D、AgCl在水溶液中难导电,但熔融状态下能导电,所以AgCl是电解质 |
下列两种气体的原子数一定相等的是( )
| A、质量相等、密度不等的N2和C2H4 |
| B、等体积等密度的CO和N2 |
| C、等温等体积的O2和Cl2 |
| D、等压等体积的NH3和CO2 |
 巳知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似:则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为( )
巳知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似:则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为( )