题目内容
可逆反应3A(g)+2B(g)?C(g)+2D(g)中,取3molA和2mol B置于2L密闭容器内,1min 后测得容器内A 的浓度减少0.15mol/L,这时B的浓度为 mol/L,D的浓度为 mol/L,这段时间内反应的平均速率若以物质A的浓度变化来表示,应为 .
考点:化学平衡的计算
专题:化学平衡专题
分析:根据三段式计算出1min时各组分的物质的量,根据浓度c=
,速率v=
计算,即可解答.
| n |
| V |
| △c |
| △t |
解答:
解:2L密闭容器内,1min 后测得容器内A 的浓度减少0.15mol/L,A的物质的量减小量为0.3mol,
3A(g)+2B(g)?C(g)+2D(g)
起始(mol) 3 2 0 0
变化(mol) 0.3 0.2 0.1 0.2
1min(mol) 2.7 1.8 0.1 0.2
此时,B的浓度c=
=
=0.9mol/L,
D的浓度c=
=
=0.1mol/L,
以物质A的浓度变化来表示平均速率v=
=
=0.15mol/(L?min),
故答案为:0.9;0.1;0.15mol/(L?min).
3A(g)+2B(g)?C(g)+2D(g)
起始(mol) 3 2 0 0
变化(mol) 0.3 0.2 0.1 0.2
1min(mol) 2.7 1.8 0.1 0.2
此时,B的浓度c=
| n |
| V |
| 1.8mol |
| 2L |
D的浓度c=
| n |
| V |
| 0.2mol |
| 2L |
以物质A的浓度变化来表示平均速率v=
| △c |
| △t |
| ||
| 1min |
故答案为:0.9;0.1;0.15mol/(L?min).
点评:本题考查了化学平衡的有关计算问题,根据三段式计算物质的量,根据浓度、反应速率公式计算即可,难度不大.

练习册系列答案
相关题目
下列各组离子一定能大量共存的是( )
| A、在强碱性溶液中:NH4+、Ag+、NO3-、I- |
| B、在pH=12的溶液中:Na+、K+、AlO2-、CO32- |
| C、在c(H+)=0.1 mol?L-1的溶液中:Ca2+、Fe2+、ClO-、Cl- |
| D、在强酸性溶液中:Mg2+、Al3+、HCO3-、SO42- |
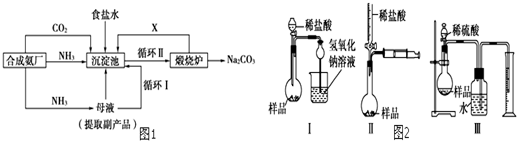
 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如表:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图.加热某废塑料得到的产物如表: