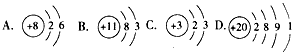题目内容
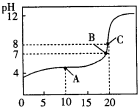
某元素A的原子,其L层比M层多5个电子,它的硫酸盐与氢氧化钠溶液反应得到白色絮状沉淀,当继续加氢氧化钠溶液时,沉淀又消失;将一部分沉淀加入盐酸时沉淀也消失.此A元素的元素符号为________,它的氢氧化物具有________,写出它与酸和碱反应的离子方程式________,________.元素B能与A形成化合物,该化合物中各原子的最外层电子数之和为24,将此化合物与浓H2SO4共热,将产生的气体通入AgNO3溶液有不溶于稀HNO3的白色沉淀产生,则B元素符号为________,写出此过程中的离子方程式:________.C元素与B元素形成CB型化合物,其中C占39.32%.又知C元素原子中有12个中子,则此C元素符号为________.
答案:
解析:
解析:
|
Al,两性,Al(OH)3+OH-= |

练习册系列答案
相关题目