题目内容
4.NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 常温常压下,11.2L 氮气所含的原子数目为NA | |
| B. | 在反应3SiO2+6C+2N2=Si3N4+6CO,生成1 mol Si3N4时共转移12 NA电子 | |
| C. | 1molNa2O2固体中含离子总数为4 NA | |
| D. | 25℃时pH=13的NaOH溶液中含有Na+的数目为0.1NA |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、反应3SiO2+6C+2N2=Si3N4+6CO转移12mol电子;
C、过氧化钠由2个钠离子和1个过氧根构成;
D、溶液体积不明确.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氮气的物质的量小于0.5mol,则含有的原子数小于NA个,故A错误;
B、反应3SiO2+6C+2N2=Si3N4+6CO中碳元素的价态由0价升高为+2价,故反应转移12mol电子,生成1molSi3N4,则当生成1 mol Si3N4时共转移12 NA电子,故B正确;
C、过氧化钠由2个钠离子和1个过氧根构成,故1mol过氧化钠中含2mol钠离子和1mol过氧根即3mol离子即3NA个,故C错误;
D、溶液体积不明确,故溶液中的钠离子的个数无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
14.以强制弱是物质世界的普遍规律.已知:四种物质的氧化能力Cl2>Br2>FeCl3>I2,下列氧化还原反应不能发生的是( )
| A. | 2I-+Cl2═I2+2Cl- | B. | 2Br-+Cl2═Br2+2Cl- | ||
| C. | Br2+2I-═2Br-+I2 | D. | 2Fe2++I2═2Fe3++2I- |
15.下列离子分别加入H2O中,基本上不影响水的电离平衡的是( )
①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO${\;}_{3}^{-}$ ⑧NH${\;}_{4}^{+}$.
①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO${\;}_{3}^{-}$ ⑧NH${\;}_{4}^{+}$.
| A. | ①③⑤⑦⑧ | B. | ②④⑦ | C. | ①⑥ | D. | ②④⑥⑧ |
19.下列描述中,错误的是( )
| A. | 往下水道中倾倒硫酸铜溶液,会进一步加快铁制管道的腐蚀 | |
| B. | 镁与稀盐酸反应剧烈,加入醋酸钠晶体可以减慢反应速率 | |
| C. | 电解饱和食盐水制氯气时用铁作阳极 | |
| D. | 电解法精炼粗铜,用纯铜作阴极 |
9.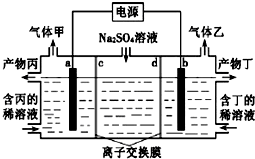 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H2O+2e-═2OH-+H2↑ |
14.下列说法或表示方法正确的是( )
| A. | 等质量的硫蒸汽和硫固体分别在氧气中完全燃烧,后者放出的热量少 | |
| B. | 1molH2在足量氯气中完全燃烧所放出的热量,是H2的燃烧热 | |
| C. | HCl与NaOH反应的中和热△=-57.3kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=-2×(-57.3)kJ•mol-1 | |
| D. | 一定条件下,0.2molSO2(g)与0.1molO2(g)混合充分反应时放出的热量为18kJ,则有SO2(g)+O2(g)═2SO3(g)△H=-180kJ•mol-1 |
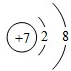 可知,氮原子最外层电子数目为5
可知,氮原子最外层电子数目为5