题目内容
下列可作为判断S和Cl的非金属性强弱依据的是( )
| A、Cl2+H2S=S↓+2Cl- | B、酸性:H2SO4<HClO | C、酸性:H2S<HCl | D、硫原子的最外层电子数比氯原子的少 |
分析:利用非金属与氢气化合的难易程度、气态氢化物的稳定性、最高价氧化物的水化物的酸性、非金属单质之间的置换反应、与变价金属反应根据生成物质金属的价态高低等来判断非金属性的强弱,以此来解答.
解答:解:A.非金属性强的单质置换非金属性弱,已知Cl2+H2S=S↓+2Cl-,所以可作为判断S和Cl的非金属性强弱依据,故A正确;
B.最高价含氧酸的酸性越强,则非金属性越强,HClO不是最高价含氧酸,所以不能作为判断S和Cl的非金属性强弱依据,故B错误;
C.不能根据氢化物的酸性强弱,来比较Cl、S元素的非金属性强弱,故C错误;
D.不能根据元素原子的最外层电子数来判断非金属性强弱,故D错误;
故选A.
B.最高价含氧酸的酸性越强,则非金属性越强,HClO不是最高价含氧酸,所以不能作为判断S和Cl的非金属性强弱依据,故B错误;
C.不能根据氢化物的酸性强弱,来比较Cl、S元素的非金属性强弱,故C错误;
D.不能根据元素原子的最外层电子数来判断非金属性强弱,故D错误;
故选A.
点评:本题考查非金属性的比较,题目难度不大,注意归纳非金属性比较的常见方法即可解答,注重规律性知识的应用来解答.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
(9分)某温度下,在2L容器中3种物质间进行反应, X、Y、Z的物质的量随时间的变化曲线如图。反应在t1min时到达平衡,依图所示: K^S*5U.C#O%
K^S*5U.C#O%
⑴①该反应的化学方程式是_____________________。
②在t1min时,该反应达到了__________状态,下列可作
为判断反应已达到该状态的是________ __(填序号)。
| A.X、Y、Z的反应速率相等 | B.X、Y的物质的量浓度不再改变 |
| C.生成3molY的同时生成1molZ | D.生成1molZ的同时生成2molX |
___________ ___。
②甲、乙两位同学讨论放热反应和吸热反应:甲说加热后才能发生的化学反应是吸热反应;乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是_ ____同学。
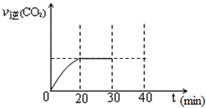 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.