题目内容
在下列三个反应中:①SO2+2NaOH=Na2SO3+H2O
②SO2+2H2S=3S↓+2H2O
③SO2+Cl2+2H2O=H2SO4+2HCl
二氧化硫所起的作用是( )
②SO2+2H2S=3S↓+2H2O
③SO2+Cl2+2H2O=H2SO4+2HCl
二氧化硫所起的作用是( )
| A.相同 | B.不同 |
| C.均是氧化剂的作用 | D.均是还原剂作用 |
①在反应SO2+2NaOH=Na2SO3+H2O中,生成盐,且硫元素的化合价不变,二氧化硫作酸性氧化物;
②在反应SO2+2H2S=3S↓+2H2O中,二氧化硫中硫元素的化合价由+4价降低为0,则二氧化硫作氧化剂;
③在反应SO2+Cl2+2H2O=H2SO4+2HCl中,二氧化硫中硫元素的化合价由+4价升高到+6价,则二氧化硫作还原剂;
显然三个反应中二氧化硫所起的作用不同,
故选B.
②在反应SO2+2H2S=3S↓+2H2O中,二氧化硫中硫元素的化合价由+4价降低为0,则二氧化硫作氧化剂;
③在反应SO2+Cl2+2H2O=H2SO4+2HCl中,二氧化硫中硫元素的化合价由+4价升高到+6价,则二氧化硫作还原剂;
显然三个反应中二氧化硫所起的作用不同,
故选B.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
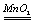 2H2O+O2↑ ③H2O2+C12==2HCl+O2↑
2H2O+O2↑ ③H2O2+C12==2HCl+O2↑