题目内容
用Pt电极电解1000mL含KNO3和Cu(NO3)2混合溶液一段时间,在两极均生成标准状况下的气体11.2L.求原混合溶液中Cu2+的物质的量浓度和电解后溶液中的H+的物质的量浓度(设电解后溶液体积不变). .
分析:阳极溶液中离子放电顺序书写电极反应,溶液中阴离子氢氧根离子失电子生成氧气,阳离子放电顺序Cu2+>H+,阳极电极反应为:4OH--4e-═2H2O+O2↑,阴极电极反应为:Cu2++2e-═Cu,2H++2e-═H2↑,依据两极生成气体物质的量结合电解过程中电子守恒计算得到.
解答:解:阳极溶液中离子放电顺序书写电极反应,溶液中阴离子氢氧根离子失电子生成氧气,阳离子放电顺序Cu2+>H+,
阳极电极反应为:4OH--4e-═2H2O+O2↑,阴极电极反应为:Cu2++2e-═Cu,2H++2e-═H2↑,
在两极均生成11.2L标准状况下的气体物质的量为0.5mol,依据电子守恒电极转移电子为4×0.5mol=2mol,生成氢气转移电子1mol,铜离子得到电子1mol,反应的铜离子物质的量0.5mol,
所以Cu2+的物质的量浓度=
=0.5mol/L,
电解后溶液中的H+的物质的量浓度依据氢氧根离子和氢离子守恒计算得到,电子转移共2mol,阳极消耗氢氧根离子物质的量为2mol,
溶液中增加氢离子物质的量为2mol,阴极上消耗氢离子1mol,
所以溶液中增加氢离子物质的量为1mol,
溶液中氢离子浓度=
=1mol/L;
答:原混合溶液中Cu2+的物质的量浓度和电解后溶液中的H+的物质的量浓度分别为0.5mol?L-1,1.0mol?L-1;
阳极电极反应为:4OH--4e-═2H2O+O2↑,阴极电极反应为:Cu2++2e-═Cu,2H++2e-═H2↑,
在两极均生成11.2L标准状况下的气体物质的量为0.5mol,依据电子守恒电极转移电子为4×0.5mol=2mol,生成氢气转移电子1mol,铜离子得到电子1mol,反应的铜离子物质的量0.5mol,
所以Cu2+的物质的量浓度=
| 0.5mol |
| 1L |
电解后溶液中的H+的物质的量浓度依据氢氧根离子和氢离子守恒计算得到,电子转移共2mol,阳极消耗氢氧根离子物质的量为2mol,
溶液中增加氢离子物质的量为2mol,阴极上消耗氢离子1mol,
所以溶液中增加氢离子物质的量为1mol,
溶液中氢离子浓度=
| 1mol |
| 1L |
答:原混合溶液中Cu2+的物质的量浓度和电解后溶液中的H+的物质的量浓度分别为0.5mol?L-1,1.0mol?L-1;
点评:本题考查了电极原理的计算应用,主要是混合电解过程中电子守恒的计算应用,掌握电解反应实质和电极反应计算是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
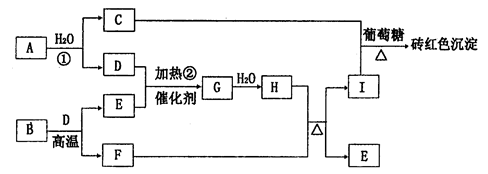
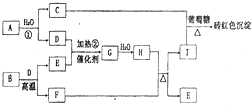 (2011?郑州二模)如图为物质A?I的转化关系(部分反应物、生成物没有列出).其中B为某金屑矿的主要成分,经过一系列反应可得到E和F.D、E常温下为气体,D、F为常见单质,
(2011?郑州二模)如图为物质A?I的转化关系(部分反应物、生成物没有列出).其中B为某金屑矿的主要成分,经过一系列反应可得到E和F.D、E常温下为气体,D、F为常见单质,