题目内容
在反应 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,被氧化与未被氧化的HCl的质量之比为( )
| A、1:1 | B、8:5 |
| C、5:8 | D、5:3 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,化合价升高的Cl元素被氧化,对应产物Cl2是氧化产物,化合价降低的Mn元素被还原,所在的反应物KMnO4是氧化剂,发生还原反应,对应产物MnCl2是还原产物,在反应的16HCl(浓)中,被氧化的占10mol,未被氧化的HCl为6mol,以此来解答.
解答:
解:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,化合价升高的Cl元素被氧化,对应产物Cl2是氧化产物,由原子守恒可知,在反应的16HCl(浓)中,被氧化的占10mol,未被氧化的HCl为6mol,被氧化与未被氧化的HCl的物质的量比等于质量比,被氧化与未被氧化的HCl的质量之比为10:6=5:3,
故选D.
故选D.
点评:本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化及原子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
只用水就能鉴别的一组物质是( )
| A、苯酚、乙醇、甘油 |
| B、乙醇、己烯、苯磺酸 |
| C、乙醛、乙二醇、硝基苯 |
| D、苯、乙醇、四氯化碳 |
在实验室里进行分液操作,下列实验仪器中一定需要使用的是( )
| A、容量瓶 | B、分液漏斗 |
| C、玻璃棒 | D、温度计 |
实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别是( )
| A、1000mL,212g |
| B、950mL,543.4g |
| C、950mL,572g |
| D、500mL,286g |
在体积相同的A、B两个带活塞的玻璃容器中,分别注入
体积颜色相同的NO2与溴蒸气,然后将活塞同时向外拉出到
(快速),过一会可以看到( )
| 1 |
| 4 |
| 1 |
| 2 |
| A、A中的颜色比B中的浅 |
| B、A中的颜色比B中的深 |
| C、A中的颜色与B中的深浅相同 |
| D、A中颜色比开始时深 |
 ③
③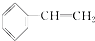 ④
④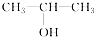 ⑤
⑤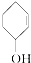 ⑥
⑥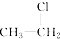
 ⑧
⑧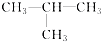 ⑨
⑨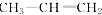 ⑩
⑩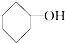 ?
? ?CH3Cl
?CH3Cl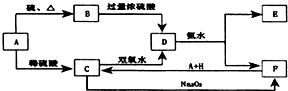 中学化学中几种常见物质的转化关系如图所示:
中学化学中几种常见物质的转化关系如图所示: