题目内容
19.在一定条件下,完全分解下列某化合物2g,产生氧气1.8g,此化合物是( )| A. | 1H216O | B. | 1H218O | C. | 2H216O | D. | 2H218O |
分析 根据质量守恒定律知,水分解生成氢气的质量为2g-1.8g=0.2g,设氧气的摩尔质量为xg/mol、氢气的摩尔质量为yg/mol,氧气的物质的量与氢气的物质的量之比为=$\frac{1.8g}{xg/mol}$:$\frac{0.2g}{yg/mol}$=1:2,据此分析解答.
解答 解:在一定条件下,完全分解下列某化合物2g,产生氧气1.8g,根据质量守恒定律知,水分解生成氢气的质量为:2g-1.8g=0.2g,
设氧气的摩尔质量为xg/mol、氢气的摩尔质量为yg/mol,
氧气的物质的量与氢气的物质的量之比为:$\frac{1.8g}{xg/mol}$:$\frac{0.2g}{yg/mol}$=1:2,整理可得:x=18y,
则氧核素为18O、氢核素为1H,二者形成的水为1H218O,
故选B.
点评 本题考查化学方程式的有关计算,侧重分析计算能力考查,明确分子构成及物质之间关系是解本题关键,题目难度不大,注意核素相对原子质量与其摩尔质量在数值上相等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A. | 将水加热,Kw增大,pH不变 | |
| B. | 向水中加入少量盐酸,c(H+)增大,Kw不变 | |
| C. | 向水中加入NaOH固体,平衡逆向移动,c(OH-)降低 | |
| D. | 向水中加入AlCl3固体,平衡正向移动,c(OH-)增大 |
10.以下对未知溶液成分的检验中,结论正确的是( )
| 实验操作 | 实验现象 | 实验结论 | |
| A | 加入盐酸 | 产生无色气体 | 溶液中一定含有CO32- |
| B | 加入KSCN溶液 | 显血红色 | 溶液中一定含有Fe3+ |
| C | 加入盐酸酸化的氯化钡溶液 | 生成白色沉淀 | 溶液中一定含有SO42- |
| D | 取未知溶液进行焰色反应 | 火焰显黄色 | 溶液中一定含有K+ |
| A. | A | B. | B | C. | C | D. | D |
7.提出元素周期律并首先运用元素周期律预测元素性质的科学家是( )
| A. | 戴维 | B. | 阿伏加德罗 | C. | 门捷列夫 | D. | 道尔顿 |
14.从柑橘中可提炼出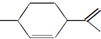 .下列关于它的说法不正确的是( )
.下列关于它的说法不正确的是( )
 .下列关于它的说法不正确的是( )
.下列关于它的说法不正确的是( )| A. | 分子式为C10H16 | |
| B. | 1mol该有机物能与4mol H2发生加成反应 | |
| C. | 能与溴水发生加成反应 | |
| D. | 常温下呈液态,难溶于水 |
4.测定1mol气体体积的实验中,下列说法正确的是( )
| A. | 硫酸过量或者镁带过量 | |
| B. | 液体量瓶中液体体积数就是气体的体积 | |
| C. | 须记录实验的环境温度 | |
| D. | 加入稀硫酸的量应恰好与镁带完全反应 |
11.下列物质中,不属于烃类的是( )
| A. | C6H6 | B. | C2H6 | C. | C2H4 | D. | C6H5OH |
8.下列操作中不影响测定1mol氢气体积的实验结果的是( )
| A. | 镁带称量后,用砂纸擦去氧化膜 | B. | 硫酸稍过量 | ||
| C. | 液体量瓶的体积读数为氢气的体积 | D. | 操作中装置漏气 |
9.下列说法正确的是??( )
| A. | 麻黄碱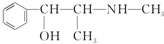 的催化氧化产物能发生银镜反应 的催化氧化产物能发生银镜反应 | |
| B. | 可用碘水和银氨溶液鉴别葡萄糖、麦芽糖和淀粉三种物质 | |
| C. | 油脂在人体内的化学变化主要是在脂肪酶的催化下进行水解 | |
| D. | 苯和油脂均不能使酸性高锰酸钾溶液褪色 |