题目内容
H2O2是实验室常用的一种化学试剂.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol?L-1FeCl3溶液 |
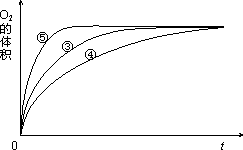
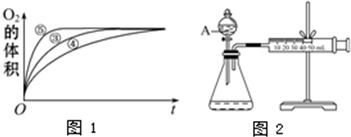
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析下图能够得出的结论是
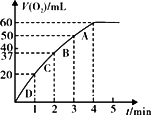
(3)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,则实验中需要测量的数是
(4)H2O2能氧化H2SO4 酸化的FeSO4,离子方程式为
分析:(1)根据实验①和②的浓度不同进行判断;
(2)由图可知,⑤的反应速率最大,④的反应速率最小,以此来解答;
(3)该反应是通过反应速率分析的,所以根据v=
分析;
(4)根据双氧水在酸性条件下将亚铁离子氧化成铁离子写出反应的离子方程式.
(2)由图可知,⑤的反应速率最大,④的反应速率最小,以此来解答;
(3)该反应是通过反应速率分析的,所以根据v=
| △v |
| △t |
(4)根据双氧水在酸性条件下将亚铁离子氧化成铁离子写出反应的离子方程式.
解答:解:(1)实验①和②的浓度不同,则该实验的目的为探究浓度对化学反应速率的影响,
故答案为:探究H2O2溶液的浓度的变化对分解速率的影响;
(2)由图可知,⑤的反应速率最大,④的反应速率最小,结合实验方案可知,碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率,
故答案为:图象显示FeCl3溶液的催化作用,碱性条件下效果较好,酸性条件下效果较弱;
(3)根据v=
知,还需要测定产生40mL气体所需的时间,
故答案为:测量出分别在Fe3+和Cu2+的催化作用下,收集40mL气体的始、终时间,就能计算出反应速率;
(4)H2O2能氧化H2SO4 酸化的FeSO4,反应生成了硫酸铁和水,反应的离子方程式为:Fe2++2H2O2+4H+═Fe3++4H2O,
故答案为:Fe2++2H2O2+4H+═Fe3++4H2O.
故答案为:探究H2O2溶液的浓度的变化对分解速率的影响;
(2)由图可知,⑤的反应速率最大,④的反应速率最小,结合实验方案可知,碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率,
故答案为:图象显示FeCl3溶液的催化作用,碱性条件下效果较好,酸性条件下效果较弱;
(3)根据v=
| △v |
| △t |
故答案为:测量出分别在Fe3+和Cu2+的催化作用下,收集40mL气体的始、终时间,就能计算出反应速率;
(4)H2O2能氧化H2SO4 酸化的FeSO4,反应生成了硫酸铁和水,反应的离子方程式为:Fe2++2H2O2+4H+═Fe3++4H2O,
故答案为:Fe2++2H2O2+4H+═Fe3++4H2O.
点评:本题考查影响化学反应速率的因素,较好的考查学生实验设计、数据处理、图象分析的综合能力,难度中等,注意信息的利用即可解答.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
H2O2是实验室常用的一种化学试剂.
I.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)实验①和②的目的是 ,实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是 .
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析图能1够得出的实验结论是 .

Ⅱ.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
(1)实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,则实验中需要测量的数据是 .
(2)加入0.1g mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示.解释反应速率变化的原因 ,计算H2O2的初始物质的量浓度 .(保留两位有效数字)
I.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol?L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol?L-1FeCl3溶液 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析图能1够得出的实验结论是

Ⅱ.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如图2所示的实验装置进行实验.
(1)实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略,则实验中需要测量的数据是
(2)加入0.1g mol MnO2粉末于50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示.解释反应速率变化的原因
H2O2是实验室常用的一种化学试剂。某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。分析下图能够得出的结论是 。
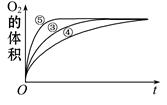
(3)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如下图所示的实验装置进行实验。
实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,则实验中需要测量的数是 。

(4)H2O2能氧化H2SO4 酸化的FeSO4,离子方程式为 ;
H2O2是实验室常用的一种化学试剂。某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
|
实验编号 |
反应物 |
催化剂 |
|
① |
10mL2% H2O2溶液 |
无 |
|
② |
10mL5% H2O2溶液 |
无 |
|
③ |
10mL5% H2O2溶液 |
1mL0.1mol·L-1FeCl3溶液 |
|
④ |
10mL5% H2O2溶液+少量HCl溶液 |
1mL0.1mol·L-1FeCl3溶液 |
|
⑤ |
10mL5% H2O2溶液+少量NaOH溶液 |
1mL0.1mol·L-1FeCl3溶液 |
(1)实验①和②的目的是_ ,
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。分析下图能够得出的结论是 。

(3)为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学设计了如下图所示的实验装置进行实验。
实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,则实验中需要测量的数是 。

(4)H2O2能氧化H2SO4 酸化的FeSO4,离子方程式为 ;