题目内容
意大利科学家使用普通氧分子和带正电的氧离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子.
(1)下列有关O4的说法正确的是:
A.O4分子内存在极性共价键
B.合成O4的反应可看作核聚变反应,不属于化学变化
C.O4与O3、O2都是氧的同素异形体
(2)制备含O2-、O22-甚至O2+的化合物都是可能的,通常它们是在氧分子进行下列各种反应时生成的:上述变化中, (填序号)相当于氧分子被氧化; (填序号)相当于氧分子被还原.

(3)写出O22-的电子式:
(4)O2+、O2-中的电子数分别为: 、 .
(1)下列有关O4的说法正确的是:
A.O4分子内存在极性共价键
B.合成O4的反应可看作核聚变反应,不属于化学变化
C.O4与O3、O2都是氧的同素异形体
(2)制备含O2-、O22-甚至O2+的化合物都是可能的,通常它们是在氧分子进行下列各种反应时生成的:上述变化中,

(3)写出O22-的电子式:
(4)O2+、O2-中的电子数分别为:
考点:同素异形体,极性键和非极性键
专题:信息给予题
分析:(1)A.根据同非金属元素的原子之间不能形成极性共价键判断;
B.合成O4的反应中元素种类不变,属于化学变化;
C.由同种元素组成的不同单质,属于同素异形体;
(2)元素化合价升高,被氧化; 元素化合价降低,被还原;
(3)O22-的电子式为: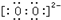 ;
;
(4)O2+、O2-中的电子数分别为:8×2-1=15、8×2+1=17.
B.合成O4的反应中元素种类不变,属于化学变化;
C.由同种元素组成的不同单质,属于同素异形体;
(2)元素化合价升高,被氧化; 元素化合价降低,被还原;
(3)O22-的电子式为:
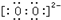 ;
;(4)O2+、O2-中的电子数分别为:8×2-1=15、8×2+1=17.
解答:
解:(1)A.同非金属元素的原子之间只能形成非极性共价键,故A错误;
B.合成O4的反应中元素种类不变,属于化学变化,故B错误;
C.O4与O3、O2都是氧元素组成的不同单质,属于同素异形体,故C正确;
故答案为:C;
(2)由氧气制备含O2+的变化中,元素化合价升高,相当于氧分子被氧化; 制备含O2-、O22-的变化中,元素化合价降低,相当于氧分子被还原,故答案为:②;①③;
(3)O22-的电子式为: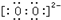 ,故答案安为:
,故答案安为: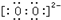 ;
;
(4)O2+、O2-中的电子数分别为:8×2-1=15、8×2+1=17,故答案为:15;17.
B.合成O4的反应中元素种类不变,属于化学变化,故B错误;
C.O4与O3、O2都是氧元素组成的不同单质,属于同素异形体,故C正确;
故答案为:C;
(2)由氧气制备含O2+的变化中,元素化合价升高,相当于氧分子被氧化; 制备含O2-、O22-的变化中,元素化合价降低,相当于氧分子被还原,故答案为:②;①③;
(3)O22-的电子式为:
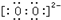 ,故答案安为:
,故答案安为: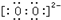 ;
;(4)O2+、O2-中的电子数分别为:8×2-1=15、8×2+1=17,故答案为:15;17.
点评:本题考查了同素异形体、极性键和非极性键等知识,难度不大.

练习册系列答案
相关题目
 科学家发现的钇钡铜氧化合物在90K具有超导性,若该化合物晶体的晶胞结构如图所示,则该化合物的化学式可能是( )
科学家发现的钇钡铜氧化合物在90K具有超导性,若该化合物晶体的晶胞结构如图所示,则该化合物的化学式可能是( )| A、YBa2Cu3O3.25 |
| B、YBa2Cu3O5 |
| C、YBa2Cu2O5 |
| D、YBaCu2O3.25 |
把镁条投入到盛有盐酸的敞口容器中,在下列因素中对产生H2速率没有影响的是( )
| A、Cl-的浓度 |
| B、镁条的表面积 |
| C、溶液的温度 |
| D、H+的浓度 |