题目内容
11.“可燃冰”是天然气与水相互作用形成的晶体物质,主要存在于冻土层和海底大陆架中.据测定每0.1m3固体“可燃冰”要释放20m3的甲烷气体,“可燃冰”将成为人类的后续能源.“可燃冰”(用甲烷表示)燃烧的化学反应方程式为:CH4+2O2→CO2+2H2O,若把该反应在一定条件下改装成原电池,则在原电池的负极发生反应的物质是:CH4.分析 “可燃冰”(用甲烷表示)燃烧即甲烷与氧气反应生成二氧化碳和水,若把该反应在一定条件下改装成原电池,则在原电池的负极发生反应的物质是失电子的氧化反应,据此分析解答.
解答 解:“可燃冰”(用甲烷表示)燃烧即甲烷与氧气反应生成二氧化碳和水,方程式为:CH4+2O2→CO2+2H2O,若把该反应在一定条件下改装成原电池,则CH4发生的是失电子的氧化反应,为负极,故答案为:CH4+2O2→CO2+2H2O;CH4.
点评 本题主要考查了可燃冰的性质以及原电池的设计,抓住原电池的原理即负极失电子发生氧化反应,正极得电子发生还原反应设计即可,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.已知25℃时Agl饱和溶液中c(Ag+)为1.22×10-6mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-6mol/L.若在5mL含有KCl和KI各为0.01mol/L的溶液中,加入8mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是( )
| A. | c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) | B. | c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | ||
| C. | c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) | D. | c(K+)>c(NO3-)>c(Ag+)=(Cl-)+c(I-) |
6.由铜、锌和稀硫酸组成的原电池中,下列各叙述正确的是( )
| A. | 溶液pH由大变小 | B. | 负极附近Zn2+浓度逐渐增大 | ||
| C. | H+向负极移动 | D. | 溶液中H2SO4的浓度不变 |
16.X+和Y2-具有与氩原子相同的电子层结构,下列叙述正确的是( )
| A. | X的原子序数比Y的小 | B. | X原子的最外层电子数比Y的大 | ||
| C. | X和Y原子的电子层数相等 | D. | X的原子半径比Y的大 |
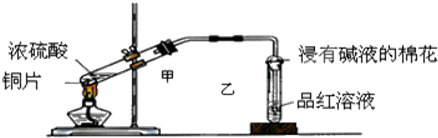
3.下列装置或操作不能达到实验目的是( )
| A. |  铁丝的析氢腐蚀实验 | B. | 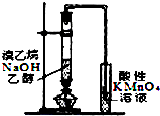 检验该反应的有机产物 | ||
| C. | 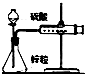 结合秒表测量锌与硫酸的反应速率 | D. | 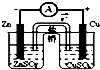 验证化学能转化为电能 |
20.不能用磨口玻璃瓶贮存的一组物质是( )
| A. | 溴水 氯水 碘水 | B. | 氢溴酸 盐酸 氢硫酸 | ||
| C. | 浓硫酸 浓硝酸 浓盐酸 | D. | NaOH溶液 Na2CO3溶液 水玻璃 |
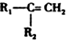 $\stackrel{HBr/过氧化物}{→}$
$\stackrel{HBr/过氧化物}{→}$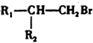 ②
②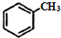 $\stackrel{KMnO/H-}{→}$
$\stackrel{KMnO/H-}{→}$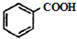
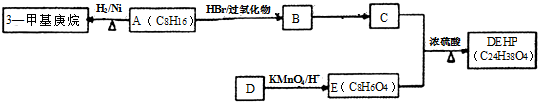
 ;反应类型:取代反应;
;反应类型:取代反应;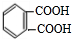 ;DEHP的结构简式是
;DEHP的结构简式是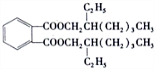 ;
;