��Ŀ����
������Ksp��AgCl��=1.56��10-10, Ksp��AgI��=1.0��10-16,���������AgCl��AgI�ı�����Һ����ҹ��ϣ��������м���һ������AgNO3���壬����˵����ȷ����
- A.����ҹ��ϣ�AgCl��AgI��������
- B.��AgCl��ҹ����AgNO3���壬c��Ag+������Ksp��AgCl��Ҳ����
- C.��AgNO3����������AgCl��AgI���ɳ���������AgCl����Ϊ��
- D.��ȡ0.235��AgI�������100ml����������仯����c��I-��=0.01mol/l
C
���������A���������AgCl��AgI�ı�����Һ����ҹ��ϣ��������м���һ������AgNO3����,��һ��AgCl��AgI��������Ҫ��Ũ����Qc�����Ksp�Ĵ�С��ϵ�����Qc>Ksp�����ɳ�������֮�������ɳ���������A����B����AgCl��ҹ����AgNO3���壬c��Ag+��������Ksp��AgCl�����䣬����ֻ���¶��йأ�����B����C����AgNO3����������AgCl��AgI���ɳ�����������ͬ����ı�����Һ�У��⻯���ܽ��ԶС���Ȼ�����������AgCl����Ϊ��������C��ȷ D����ȡ0.235��AgI�������100ml����������仯����c��I-��=0.01mol/l��Qc=1.0��10-4>Ksp��AgI�������Ի������ɳ����ķ����ƶ���c��I-��<0.01mol/l������D������ѡC��
���㣺Ũ������������ƽ�ⳣ��Ksp�Ĺ�ϵ
���������ӵ�Ũ���̣�Qc��ָ��һ����������Ũ���ݵij˻���c��ʾ����ʱ�̵�Ũ�ȣ�������ƽ��ʱ��Ҳ���Dz�ƽ��ʱ��Ũ�ȣ�Ũ����ֻ������Ũ���йأ������������ء�
ͨ���Ƚ�Ksp��IP�Ĵ�С����ȷ���Ƿ��г������ɻ�����Ƿ��ܽ⡣Ksp<Qc�����г���������Ksp=Qc���ﵽƽ�⣻Ksp>Qc����������������ܽ⣬��������Ũ������������ƽ�ⳣ��Ksp�Ĺ�ϵ�����ܽ���������⡣
���������A���������AgCl��AgI�ı�����Һ����ҹ��ϣ��������м���һ������AgNO3����,��һ��AgCl��AgI��������Ҫ��Ũ����Qc�����Ksp�Ĵ�С��ϵ�����Qc>Ksp�����ɳ�������֮�������ɳ���������A����B����AgCl��ҹ����AgNO3���壬c��Ag+��������Ksp��AgCl�����䣬����ֻ���¶��йأ�����B����C����AgNO3����������AgCl��AgI���ɳ�����������ͬ����ı�����Һ�У��⻯���ܽ��ԶС���Ȼ�����������AgCl����Ϊ��������C��ȷ D����ȡ0.235��AgI�������100ml����������仯����c��I-��=0.01mol/l��Qc=1.0��10-4>Ksp��AgI�������Ի������ɳ����ķ����ƶ���c��I-��<0.01mol/l������D������ѡC��
���㣺Ũ������������ƽ�ⳣ��Ksp�Ĺ�ϵ
���������ӵ�Ũ���̣�Qc��ָ��һ����������Ũ���ݵij˻���c��ʾ����ʱ�̵�Ũ�ȣ�������ƽ��ʱ��Ҳ���Dz�ƽ��ʱ��Ũ�ȣ�Ũ����ֻ������Ũ���йأ������������ء�
ͨ���Ƚ�Ksp��IP�Ĵ�С����ȷ���Ƿ��г������ɻ�����Ƿ��ܽ⡣Ksp<Qc�����г���������Ksp=Qc���ﵽƽ�⣻Ksp>Qc����������������ܽ⣬��������Ũ������������ƽ�ⳣ��Ksp�Ĺ�ϵ�����ܽ���������⡣

��ϰ��ϵ�д�
 ��ѧ����ϵ�д�
��ѧ����ϵ�д� �ο�������ϵ�д�
�ο�������ϵ�д�
�����Ŀ
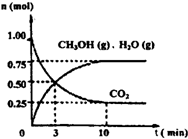 ��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���
��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���