题目内容
【题目】有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如表所示:
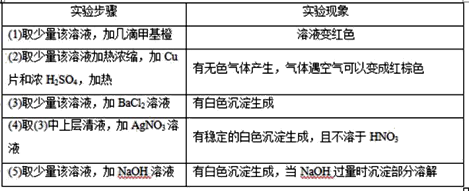
由此判断:
(1)溶液中肯定存在的离子是________________,溶液中肯定不存在的离子是________________________。
(2)为进一步确定其他离子,应该补充的实验及对应欲检离子的名称_______(如为溶液反应,说明使用试剂的名称,不必写详细操作步骤)______________________________________________________。
【答案】Al3+、Mg2+、NO3-、SO42- Fe2+、Ba2+、I-、HCO3- 焰色反应,检验K+ 稀HNO3溶液、AgNO3溶液,检验Cl-
【解析】
根据实验现象分析溶液中离子的存在情况,根据焰色反应原理分析解答。
(1) 一无色透明溶液,因为Fe2+为浅绿色,则Fe2+肯定不存在;(1)取少量该溶液,加几滴甲基橙,溶液显红色,说明溶液显示酸性,所以HCO3-不存在;且NO3-、I-不能同时存在;由(2)取少量该溶液加热浓缩,加Cu片和浓硫酸,加热有无色气体产生,气体(NO)遇空气可以变成红棕色(二氧化氮),说明溶液中含有NO3-,则一定不含有I-;由(3)取少量该溶液,加BaCl2溶液,有白色沉淀生成,则含有SO42-,原溶液中一定不存在Ba2+,由(4)取(3)中的上层清夜,加AgNO3,有稳定的白色沉淀生成,且不溶于稀硝酸,则含有Cl-,但(3)所加的氯化钡中含有Cl-,所以原离子中的Cl-是否存在不确定;由(5)取少量该溶液,加入NaOH溶液有白色沉淀生成,当NaOH过量时,沉淀部分溶解,则含有Mg2+、A13+,综上所述,一定存在Mg2+、A13+、NO3-、SO42-,肯定不存在Ba2+、I-、Fe2+、HCO3-,故答案为Al3+、Mg2+、NO3-、SO42-; Fe2+、Ba2+、I-、HCO3-;
(2) 由上述分析可知,K+、Cl-不能确定,用焰色反应确定K+存在,用原溶液、Ba(NO3)2溶液、稀HNO3和AgNO3溶液作沉淀反应来确定Cl-的存在,故答案为: 焰色反应,检验K+;稀HNO3溶液、AgNO3溶液,检验Cl-。

 阅读快车系列答案
阅读快车系列答案