题目内容
目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:3H2(g)+CO2(g)?CH3OH(g) +H2O(g),如图表示该反应进行过程中能量(单位为kJ/mol)的变化.
+H2O(g),如图表示该反应进行过程中能量(单位为kJ/mol)的变化.
①在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,下列措施中能使c(CH3OH)增大的是 (填字母)
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1mol CO2和3molH2
②当反应达到平衡时不断改变条件(但不改变各组分物质的量和状态且只改变一个条件)反应速率随时间的变化如图:其中表示平衡混合物中CH3OH含量最高的一段时间是 ;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,则K1 K2(填>、=、<).
 +H2O(g),如图表示该反应进行过程中能量(单位为kJ/mol)的变化.
+H2O(g),如图表示该反应进行过程中能量(单位为kJ/mol)的变化.①在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,下列措施中能使c(CH3OH)增大的是
a.升高温度

b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1mol CO2和3molH2
②当反应达到平衡时不断改变条件(但不改变各组分物质的量和状态且只改变一个条件)反应速率随时间的变化如图:其中表示平衡混合物中CH3OH含量最高的一段时间是
考点:化学反应速率与化学平衡图象的综合应用,化学平衡的影响因素
专题:
分析:①根据图象知,该反应的正反应是放热反应,能使c(CH3OH)增大,说明平衡向正反应方向移动;
②根据图象知,t1时刻,正逆反应速率都增大且可逆反应向逆反应方向移动,改变的条件是升高温度;t3时刻,正逆反应速率都增大且相等,改变的条件是加入催化剂;t4时刻正逆反应速率都减小,且平衡向逆反应方向移动,改变的条件是减小压强,据此分析解答.
②根据图象知,t1时刻,正逆反应速率都增大且可逆反应向逆反应方向移动,改变的条件是升高温度;t3时刻,正逆反应速率都增大且相等,改变的条件是加入催化剂;t4时刻正逆反应速率都减小,且平衡向逆反应方向移动,改变的条件是减小压强,据此分析解答.
解答:
解:①a.升高温度,平衡逆向移动,c(CH3OH)减小,故a错误;
b.充入He(g),使体系压强增大,由于容器为恒容容器,各组分浓度不变,平衡不移动,c(CH3OH)不变,故b错误;
c.将H2O(g)从体系中分离出来,平衡正向移动,c(CH3OH)增大,故c正确;
d.再充入1mol CO2和3molH2,平衡正向移动,c(CH3OH)增大,故d正确.
故答案为:cd;
②根据图象知,t1时刻,正逆反应速率都增大且可逆反应向逆反应方向移动,改变的条件是升高温度;t3时刻,正逆反应速率都增大且相等,改变的条件是加入催化剂;t4时刻正逆反应速率都减小,且平衡向逆反应方向移动,改变的条件是减小压强,所以平衡混合物中CH3OH含量最高的一段时间是t0~t1;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,且t0~t1温度小于t2~t3温度,所以K1>K2,故答案为:t0~t1;>.
b.充入He(g),使体系压强增大,由于容器为恒容容器,各组分浓度不变,平衡不移动,c(CH3OH)不变,故b错误;
c.将H2O(g)从体系中分离出来,平衡正向移动,c(CH3OH)增大,故c正确;
d.再充入1mol CO2和3molH2,平衡正向移动,c(CH3OH)增大,故d正确.
故答案为:cd;
②根据图象知,t1时刻,正逆反应速率都增大且可逆反应向逆反应方向移动,改变的条件是升高温度;t3时刻,正逆反应速率都增大且相等,改变的条件是加入催化剂;t4时刻正逆反应速率都减小,且平衡向逆反应方向移动,改变的条件是减小压强,所以平衡混合物中CH3OH含量最高的一段时间是t0~t1;如t0~t1平衡常数为K1,t2~t3平衡常数为K2,且t0~t1温度小于t2~t3温度,所以K1>K2,故答案为:t0~t1;>.
点评:本题考查化学平衡影响因素、平衡常数等知识点,侧重考查学生运用知识解答问题能力,难点是图象分析,知道外界条件改变对反应速率的影响,会正确判断平衡移动方向,难度中等.

练习册系列答案
相关题目
在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )
| A、所用NaOH已经潮解 |
| B、向容量瓶中加水未到刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、所用容量瓶不干燥 |
能一次区分乙酸、乙醇、苯、溴苯四种物质的试液的是( )
| A、水 |
| B、Na2CO3稀溶液 |
| C、银氨溶液 |
| D、稀硫酸 |
可逆反应N2+3H2?2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是( )
| A、v正(N2)=v正(H2) |
| B、v正(N2)=v逆(NH3) |
| C、2v正(H2)=3v逆(NH3) |
| D、v正(N2)=3v逆(H2) |
下列表示的是有机化合物结构式中的一部分,其中不是官能团的是( )
| A、-OH |
B、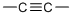 |
C、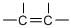 |
| D、-CH3 |
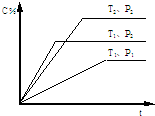 已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,下图表示在不同反应时间t 时,温度T和压强P与生成物C在混合物中的体积百分含量的关系曲线.由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,下图表示在不同反应时间t 时,温度T和压强P与生成物C在混合物中的体积百分含量的关系曲线.由曲线分析,下列判断正确的是( )| A、T1<T2,P1>P2,m+n>p,正反应吸热 |
| B、T1>T2,P1<P2,m+n>p,正反应放热 |
| C、T1<T2,P1>P2,m+n<p,正反应放热 |
| D、T1>T2,P1<P2,m+n<p,正反应吸热 |
A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、NaHSO4溶液和BaCl2溶液中的一种,已知A、B溶液的pH相同,A、C混合后溶液变浑浊.下列说法不正确的是( )
| A、D溶液的pH>7 |
| B、C溶液中的溶质溶于水促进了水的电离 |
| C、溶液A滴入到碳酸氢钠溶液中产生气体 |
| D、溶液B与NaOH共热有气体产生 |

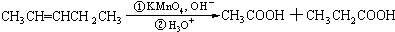
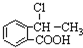 合成
合成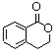 ,写出相关合成流程图(无机试剂任取).
,写出相关合成流程图(无机试剂任取).