题目内容
2.下列措施对增大反应速率明显有效的是( )| A. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| B. | Fe与稀硫酸反应制取H2时,改用浓硫酸 | |
| C. | Al在氧气中燃烧生成A12O3,将Al片改成Al粉 | |
| D. | Na与水反应时增大水的用量 |
分析 A、压强只对气体的反应速率有影响;
B、浓硫酸具有强氧化性,使铁发生钝化;
C、增大固体的接触面积能够加快反应速率;
D、钠与水反应剧烈,加水不能改变浓度.
解答 解:A、压强只对气体的反应速率有影响,对非气体的反应没有影响,增大压强速率不变,故A错误;
B、浓硫酸具有强氧化性,与铁发生钝化反应,没有氢气生成,不能提高生成气体的反应速率,故B错误;
C、将Al片改成Al粉,增大了反应物的接触面积,所以能使反应速率加快,故C正确;
D、加水不能改变浓度水的浓度,对反应速率没有影响,故D错误;
故选C.
点评 本题考查化学反应速率的影响因素,题目难度不大,注意浓硫酸与稀硫酸的性质的不同,为本题的易错点.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案
相关题目
2.Na和Na+两种粒子中,不相同的是( )
①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数.
①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数.
| A. | ①② | B. | ③④ | C. | ①②③ | D. | ②③④ |
17.下列化合物中阳离子比阴离子多1个电子层的是( )
| A. | NaCl | B. | MgBr2 | C. | CaCl2 | D. | K2O |
11.下列离子方程式书写正确的是( )
| A. | KMnO4溶液用盐酸酸化并加入H2O2:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O | |
| B. | Fe2(SO4)3和Ba(OH)2溶液混合:Fe3++SO42-+Ba2++3OH-=BaSO4↓+Fe(OH)3↓ | |
| C. | 等体积等物质的量浓度的AlCl3、Ba(OH)2、HCl溶液混合:3H++Al3++6OH-=Al(OH)3↓+3H2O | |
| D. | 水玻璃与稀醋酸混合:SiO32-+2H+=H2SiO3↓ |

 .
. .
. .
. .
.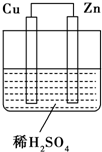 如图所示是Zn和Cu形成的原电池,其实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
如图所示是Zn和Cu形成的原电池,其实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )