题目内容
将物质的量均为a mol的钠和铝一同投入m g水中(水足量),所得溶液的密度为ρg-Cm-3,则此溶液的物质的量浓度为( )
A.
| B.
| ||||
C.
| D.
|
钠和铝投入足量水中发生反应:2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
由方程式可知,a mol的钠反应生成amol氢氧化钠,生成氢气0.5amol;amol氢氧化钠与amol铝恰好反应生成amol偏铝酸钠,同时生成氢气1.5amol.溶液为偏铝酸钠溶液.
所以氢气的质量为(0.5amol+1.5amol)×2g/mol=4ag;
所以溶液质量m(溶液)=m(金属)+m(H2O)-m(H2)=amol×23g/mol+amol×27g/mol+mg-4ag=(46a+m)g,
所以溶液的体积为
=
ml
所以溶液的物质的量浓度为
=
mol/L.
故选:C.
由方程式可知,a mol的钠反应生成amol氢氧化钠,生成氢气0.5amol;amol氢氧化钠与amol铝恰好反应生成amol偏铝酸钠,同时生成氢气1.5amol.溶液为偏铝酸钠溶液.
所以氢气的质量为(0.5amol+1.5amol)×2g/mol=4ag;
所以溶液质量m(溶液)=m(金属)+m(H2O)-m(H2)=amol×23g/mol+amol×27g/mol+mg-4ag=(46a+m)g,
所以溶液的体积为
| (46a+m)g |
| ρg/ml |
| 46a+m |
| ρ |
所以溶液的物质的量浓度为
| amol | ||
|
| 1000ρa |
| 46a+m |
故选:C.

练习册系列答案
相关题目
将物质的量均为a mol的钠和铝一同投入m g水中(水足量),所得溶液的密度为ρg·Cm-3,则此溶液的物质的量浓度为( )
| A.mol/L | B.mol/L | C.mol/L | D.mol/L |
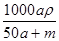 mol·L-1 B.
mol·L-1 B.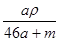 mol·L-1 C.
mol·L-1 C.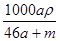 mol·L-1
D.
mol·L-1
D.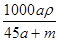 mol·L-1
mol·L-1