题目内容
[第(1)(3)(4)(6)问每空1分;(2)(5)每空2分,共13分]
粗食盐中常含有少量Ca2+、Mg2+、SO42-以及泥沙等杂质,实验室提纯NaCl的流程如下(加入的试剂稍过量)
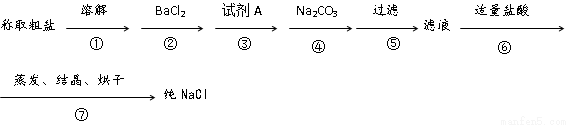
(1)步骤③中加入的试剂A是 (填化学式),其目的是 。
(2)第⑥步中,写出相应的离子方程式 。
(3)步骤⑤和⑥之间,若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是 。
(4)实验室提纯NaCl的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,其中过滤时,使用玻璃棒的目的是 。
(5)用上述方法获得的氯化钠去配制200mL0.1mol/LNaCl溶液。
①用托盘天平称氯化钠固体的质量是 g
②配制溶液需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和 。
③下列操作中,可能造成所配制溶液的浓度偏低的是 。
A、没有洗涤烧杯和玻璃棒
B、定容时,仰视刻度线读数
C、定容时,俯视刻度线读数
D、洗涤后的容量瓶中残留少量蒸馏水
(6)此方法获得的氯化钠溶液的导电性远远强于氯化钠固体,是因为氯化钠固体在水分子的作用下,电离成自由移动的离子,请写出相关的电离方程式: 。
[(1)(3)(4)(6)每空1分;(2)(5)每空2分,共13分]
(1)NaOH;除去Mg2+
(2)H++OH-=H2O
2H++CO32-  CO2↑+ H2O (每个离子方程式1分)
CO2↑+ H2O (每个离子方程式1分)
(3)在酸性条件下,BaCO3、CaCO3、Mg(OH)2会溶解,从而使制得氯化钠的混有杂质 (答案合理可得分)
(4)引流
(5)①1.2 ②200mL容量瓶 ③AB
(6)NaCl = Na++Cl-
【解析】
试题分析:(1)将粗盐溶解后,加入氯化钡溶液,目的是除去硫酸根离子,加入碳酸钠溶液,目的是除去钙离子和过量的钡离子,则步骤③中加入的试剂A是NaOH,目的是除去溶液中的Mg2+;
(2)因为除去Ca2+、Mg2+、SO42-所用试剂都是过量的,所以加入适量盐酸的目的是除去过量的氢氧根离子及碳酸根离子,发生反应的离子方程式是H++OH-=H2O 、2H++CO32-  CO2↑+ H2O;
CO2↑+ H2O;
(3)步骤⑤和⑥之间,若先用盐酸调pH再过滤,则产生的碳酸钡、氢氧化镁、碳酸钙沉淀又与盐酸反应生成氯化物,使制得的氯化钠中含有杂质;
(4)过滤使用玻璃棒,目的是起引流作用;
(5)①配制200mL0.1mol/LNaCl溶液,需要NaCl的物质的量是0.2L×0.1mol/L=0.02mol,则质量为0.02mol×58.5g/mol=1.17g,根据托盘天平的精确度,则应称量氯化钠固体的质量是1.2g;
②配制溶液需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管,还需200mL的容量瓶;
③A、未洗涤烧杯、玻璃棒,会导致溶液中氯化钠的物质的量减少,浓度偏低,正确;B、定容时,仰视刻度线读数,使所配溶液的体积偏大,所以浓度偏低,正确;C、定容时,俯视刻度线读数,使所配溶液的体积偏小,所以浓度偏高,错误;D、在配制过程中需直接向容量瓶内加水,所以容量瓶内有少量蒸馏水,对结果无影响,错误,答案选AB;
(6)氯化钠是强电解质,在水中完全电离产生氯离子和钠离子,电离方程式是NaCl = Na++Cl-。
考点:考查粗盐的除杂提纯的分析,溶液配制的计算与误差分析

 2C(g) △H<0某研究小组研究其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
2C(g) △H<0某研究小组研究其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
 2NaOH+H2↑
2NaOH+H2↑