��Ŀ����
��ĩ״����A���ɵ����ʵ�����MgO��Fe2O?��ɵĻ�����������ʵ�飺
��ȡ����A�������ȷ�Ӧ���������е���B���ɣ�
����ȡ20��Aȫ������0. 15L 6mol��L -1�������У�����ҺC��
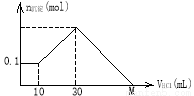
�۽����еõ��ĵ���B����ҺC��Ӧ���ų�1.12L���壨��״������ͬʱ������ҺD�����в�����������B��
����KSCN��Һ����ʱ����ҺD����ɫ��
����գ�
��1�������������ȷ�Ӧ��ʵ������� ��
�����еĵ���B�� ��
��2�������������ĸ���Ӧ�Ļ�ѧ����ʽ�� �� ��
��3�������������ĸ���Ӧ�����ӷ���ʽ�� �� ��
��4������ҺD���������Ϊ0.15L�������Һ��c��Mg2+��Ϊ ��c��Fe2+��Ϊ ��
25.��1��������������أ�����þ�����������ȼ�� Fe
��2��Fe 2O3 + 6HCl ��2 FeCl3 + 3H2O��MgO +2HCl ��MgCl2 + H2O
��3��Fe + 2H+ �� Fe2+ + H2���� 2Fe3+ + Fe �� 3 Fe2+
��4��0.67 mol/L��2�֣��� 2.3 mol/L��2�֣�
��������
�����������1�������ȷ�Ӧ��Ҫ�ڸ����½��У���Ϊþ��ȼ���ܷų��������ȣ������������ȷ�Ӧ��ʵ������Ǽ�����������أ�����þ�����������ȼ�������ȷ�Ӧ������Fe2O3��Ӧ������������������Ϊ������������أ�����þ�����������ȼ��Fe����2������Ϣ��֪��MgO��Fe2O?ȫ������0.15L 6mol��L -1�������У��������ĸ���Ӧ�Ļ�ѧ����ʽ��Fe 2O3 + 6HCl ��2 FeCl3 + 3H2O��MgO +2HCl ��MgCl2 + H2O
��3����ҺC�еijɷ�Ϊ�Ȼ�þ���Ȼ������������ᣬ���ݲ����֪���������ᷴӦ�����ݲ����֪�������Ȼ�����Ӧ���ҷ�Ӧ������в���Fe3+��ֻ��Fe��Fe2+���ʴ�Ϊ��Fe+2H+�TFe2++H2����Fe+2Fe3+�T3Fe2+; ��4����20g��A���������ʣ�MgO��Fe2O3�������ʵ�����ȣ����ƶϳ����߽�Ϊ0.1mol��0.15L 6mol/L �������У�HCl���ʵ���Ϊ0.90mol����Ӧ����0.1molMgCl2��0.2molFeCl3��0.1molHCl������n��Mg2+��=0.1mol������c��Mg2+��=0.1/0.15=0.67mol/L�����ݲ����ģ��õ���������Ӧ������в���Fe3+��ֻ��Fe��Fe2+�����ƶϳ�������B��Fe��������ҺC���µ�0.1mol���ᷴӦ��
Fe + 2HCl=FeCl2 +H2��
0.05 0.1 0.05 0.05 ��õ�0.05mol�Ȼ�������Ȼ�������Ȼ���������Ӧ��
2FeCl3 +Fe=3FeCl2
0.2 0.3 ��˷�Ӧ��ϣ�n��Fe2+ ��=0.3+0.05=0.35mol c��Fe2+ ��=2.3mol/L��
��Mg2+��Fe2+��Ũ�ȷֱ�Ϊ��0.67mol/L��2.3mol/L��
���㣺�������ȷ�Ӧ��

 2Fe��3CO2
2Fe��3CO2 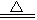 N2O��ʮ2H2O
N2O��ʮ2H2O