题目内容
12.下列说法正确的是( )| A. | 乳酸薄荷醇酯(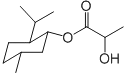 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛(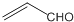 )不是同系物,它们与氢气充分反应后的产物是同系物 )不是同系物,它们与氢气充分反应后的产物是同系物 | |
| C. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| D. | CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,核磁共振氢谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用核磁共振氢谱鉴别 |
分析 A.乳酸薄荷醇酯中含有羟基,能够发生取代反应;
B.关键乙醛和丙烯醛的结构及二者与氢气反应产物判断是否属于同系物;
C.聚乙烯和苯分子中不含碳碳双键;
D.二者含有的氢原子的种类、相应的数目相同,但是各种氢原子的具体位置不同,可以用核磁共振氢谱来鉴别.
解答 解:A.乳酸薄荷醇酯( )中含有酯基、羟基,能够发生水解、氧化、消去反应,还能够发生取代反应(H氢原子被卤素原子确定),故A错误;
)中含有酯基、羟基,能够发生水解、氧化、消去反应,还能够发生取代反应(H氢原子被卤素原子确定),故A错误;
B.乙醛和丙烯醛( )的结构不同,所以二者一定不是同系物;它们与氢气充分反应后分别生成乙醇和丙醇,所以与氢气加成的产物属于同系物,故B正确;
)的结构不同,所以二者一定不是同系物;它们与氢气充分反应后分别生成乙醇和丙醇,所以与氢气加成的产物属于同系物,故B正确;
C.聚乙烯和苯分子中不含碳碳双键,故C错误;
D.CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,核磁共振氢谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,但是二者的核磁共振氢谱中峰的位置不相同,可以用核磁共振氢谱来鉴别,故D错误.
故选B.
点评 本题考查了常见有机物的结构与性质、核磁共振氢谱的应用、同系物的判断,题目难度中等,注意掌握常见有机物的结构与性质,明确核磁共振氢谱表示的意义及同系物的概念.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
16.如图中a、b、c、d为周期表前4周期的部分元素,下列叙述正确的是( )
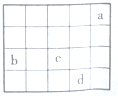

| A. | 四种元素中,d单质的化学性质最稳定 | |
| B. | 气态氢化物的还原性:d>c | |
| C. | 原子半径:b<c | |
| D. | b元素最高价氧化物可形成原子晶体 |
1.298.15K时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | c(H+)=1×10-13mol/L的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| C. | 0.1mol/LNH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
2.X、Y、Z、W、R属于短周期元素.已知它们都不是稀有气体元素,X的原子半径最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1. 下列叙述错误的是( )
| A. | X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物低 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序是:R>W>Z | |
| D. | Y分别与Z、W、R以两种元素组成的常见化合物有5种 |
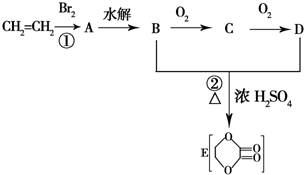 由乙烯和其他无机原料合成环状 化合物其合成过程如图(水及其他无机产物均已省略):
由乙烯和其他无机原料合成环状 化合物其合成过程如图(水及其他无机产物均已省略):
 .
. ,工业上扁桃酸可以由烃A经过以下步骤合成得到:
,工业上扁桃酸可以由烃A经过以下步骤合成得到: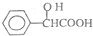
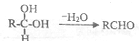
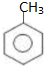 ;扁桃酸中含氧官能团名称羟基、羧基.
;扁桃酸中含氧官能团名称羟基、羧基. .
.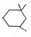 )在浓硫酸作用下反应生成,请写出反应的化学方程式
)在浓硫酸作用下反应生成,请写出反应的化学方程式
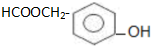 .
.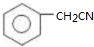 )为原料合成扁桃酸的同分异构体-对羟基苯乙酸(
)为原料合成扁桃酸的同分异构体-对羟基苯乙酸(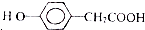 )的合理路线.
)的合理路线.