题目内容
20. 工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图:
工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图:(1)此流程的第II步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的平衡常数的表达式为$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$;反应的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是AD.
| 实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
| A | 1、1、0、0 | c1 | Q1 | α1 |
| B | 0、0、2、2 | c2 | Q2 | α2 |
| C | 2、2、0、0 | c3 | Q3 | α3 |
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是②③.
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化⑥v(CO2)正=v(H2O)
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是降低温度、增加水蒸汽的量(写出两种).若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变).

分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
由表中数据可知,随温度升高平衡常数减小,说明升高温度平衡逆向移动,而升高温度平衡向吸热反应方向移动;
设在830℃下平衡时CO的转化率为x,表示出平衡时各组分物质的量,由于反应前后气体体积不变,可以用物质的量代替浓度代入平衡常数表达式列方程计算解答;
(2)各物质起始物质的量均为1:1等于化学计量数之比,结合方程式可知,故平衡时n(CO)=n(H2O)、n(CO2)=n(H2),由于500℃时平衡常数K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$=9可知,平衡时n(CO2)≠n(CO),则转化率不是50%;
B中转化到左边可以得到2molCO、2molH2O,恒温恒容下B、C是完全等效平衡,平衡时相同物质的浓度相同、物质的量相同;
恒温恒容下,C等效为在A的基础上增大压强,反应前后气体体积不变,平衡不移动,反应物转化率相等、相同物质的含量相等;
(3)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
(4)在t2时刻后CO的浓度减小、CO2浓度增大,平衡向正反应方向移动,可以通过改变温度、改变水蒸气或氢气的量实现;
t4时刻通过改变容积的方法将压强增大为原先的两倍,则体积变为原来的一半,瞬间浓度分别增大为原来的2倍,由于反应前后气体系数相等,平衡不移动.
解答 解:(1)反应CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数的表达式K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$;
由表中数据可知,随温度升高平衡常数减小,说明升高温度平衡逆向移动,而升高温度平衡向吸热反应方向移动,则正反应是放热反应;
设在830℃下平衡时CO的转化率为x,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
起始量(mol):1 2 0 0
变化量(mol):x x x x
平衡量(mol):1-x 2-x x x
由于反应前后气体体积不变,可以用物质的量代替浓度计算平衡常数,则K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$=$\frac{x×x}{(1-x)×(2-x)}$=1,解得x=66.7%;
故答案:$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$;放;66.7%;
(2)各物质起始物质的量均为1:1等于化学计量数之比,结合方程式可知,故平衡时n(CO)=n(H2O)、n(CO2)=n(H2),由于500℃时平衡常数K=$\frac{c({H}_{2})×c(C{O}_{2})}{c(CO)×c({H}_{2}O)}$=9可知,平衡时n(CO2)≠n(CO),则转化率不是50%;
B中转化到左边可以得到2molCO、2molH2O,恒温恒容下B、C是完全等效平衡,平衡时相同物质的浓度相同、物质的量相同,则:c2=c3,B、C平衡时n(CO2)≠n(CO),转化率不是50%,故Q2≠Q3,设平衡时CO为ymol,则α3=$\frac{y}{2}$,α2=$\frac{2-y}{2}$,故α3+α2=1,可推知α3≠α2;
恒温恒容下,C等效为在A的基础上增大压强,反应前后气体体积不变,平衡不移动,反应物转化率相等、相同物质的含量相等,则:α1=α3,c3=2c1,Q3=2Q1,
结合上述分析可知:2c1=c2=c3 ,Q3=2Q1≠Q2=Q3 ,α1=α3≠α2 ,α1+α2=1,
故选:AD;
(3)①虽然反应前后气体体积不变,但由于绝热等容容器中反应过程中有温度变化,所以压强也在变化,体系的压强不再发生变化能判断反应达到平衡,故①正确;
②反应中混合气体总质量不变,容器容积不变,混合气体密度始终不变,故②错误;
③反应中混合气体总质量不变,反应前后气体的物质的量不变,混合气体的平均相对分子质量始终不变,故③错误;
④各组分的物质的量浓度不再改变是平衡的标志,故④正确;
⑤体系的温度不再发生变化绝热容器温度不变,说明反应达到平衡,故⑤正确;
⑥反应速率之比等于化学方程式计量数之比,v(CO2)正=v(H2O)逆说明水蒸气的正逆反应速率相同,反应到达平衡,故⑥正确;
故答案为:②③;
(4)在t2时刻CO的浓度减小、CO2浓度增大,平衡向正反应方向移动,且CO和CO2浓度变化有接触点,所以可以通过改变降低温度、增大水蒸气的量或减少氢气的量实现;
t4时刻通过改变容积的方法将压强增大为原先的两倍,则体积变为原来的一半,瞬间浓度分别增大为原来的2倍,由于反应前后气体系数相等,平衡不移动,在图中t4和t5区间内画出CO、CO2浓度变化曲线如图: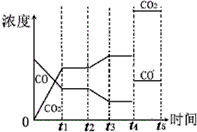 ,
,
故答案为:降低温度,或增加水蒸汽的量,或减少氢气的量; .
.
点评 本题考查化学平衡计算、化学平衡移动原理、平衡状态判断、化学平衡图象等,是对学生综合能力的考查,需要学生具备扎实的基础.

| A. | Na2HPO4+NaH2PO4 | B. | Na3PO4 | C. | NaH2PO4 | D. | Na3PO4+NaH2PO4 | ||||
| E. | Na3PO4+Na2HPO4 |
 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式,并在方框内填上系数.
□C+□KMnO4+□H2SO4=□CO2↑+□MnSO4+□K2SO4+□6H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)?CO2(g)+H2(g),得到如下二组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
(保留小数点后二位数,下同).
②实验2条件下平衡常数K=0.17,该反应为放热(填“吸热”或“放热”)反应.
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO (g)+O2(g)═2CO2(g)△H2=-566.0kJ/mol
③H2O(g)═H2O(l)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-354.8KJ/mol.
(4)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置.
①该电池正极的电极反应式为:O2+4e-+2H2O=4OH-;该电极上每消耗1.6g氧气,转移的电子数为0.2mol.
②该电池工作时,溶液中的OH-向负(填“正”或“负”)极移动.
(1)实验测得,8g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,下列热化学方程式正确的是C
A、$\frac{1}{4}$CH30H+$\frac{3}{8}$02=$\frac{1}{4}$C02+$\frac{1}{2}$H20△H=-113.5kJ•mol-1
B、$\frac{1}{4}$CH30H(l)+$\frac{3}{8}$02(g)=$\frac{1}{4}$C02(g)+$\frac{1}{2}$H20(l)△H=+113.5kJ•mol-1
C、2CH30H(l)+302(g)=2C02(g)+4H20(l)△H=-908kJ•mol-1
D、2CH30H(l)+302(g)=2C02(g)+4H20(l)△H=+908kJ•mol-1
(2)由气态基态原子形成1mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
(3)由金红石(TiO2)制备单质Ti,涉及的步骤为:TiO2-→TiCl4$→_{800℃,Ar}^{Mg}$Ti
已知:①C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g)△H=+141kJ•mol-1
则TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H=-80kJ•mol-1.
| A. | 甲烷的燃烧热△H=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 一定条件下,将0.5 mol N2和1.5 molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| C. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| D. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 molN2和1.5 molH2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | HCl和NaOH反应的中和热为-57.3 kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3 kJ•mol-1) | |
| D. | 在101 kPa时,2 gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 |
| A. | 氯水保存在棕色试剂瓶中 | B. | 漂白粉露置在空气中存放 | ||
| C. | 过氧化钠应密封保存 | D. | 金属钠保存在煤油中 |