题目内容
20.某原电池装置图如图所示,有关该原电池的说法正确的是( )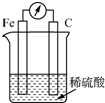
| A. | 在铁棒上产生气泡,碳棒上没有气泡 | |
| B. | H+在溶液中定向流向铁 | |
| C. | 电子由铁电极流出 | |
| D. | 该装置能将电能转化为化学能 |
分析 将化学能转变为电能的装置是原电池,铁、碳、稀硫酸构成的原电池中,铁作负极,负极上失电子发生氧化反应,碳作正极,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极.
解答 解:A.碳棒上氢离子放电生成氢气,故A错误;
B.H+在溶液中定向流向正极碳棒,故B错误;
C.电子从铁棒沿导线流向碳棒,故C正确;
D.该装置是原电池,是将化学能转变为电能的装置,故D错误.
故选C.
点评 本题考查了原电池和电解池原理,难度不大,电极反应式的书写是学习的难点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列物质中,属于电解质的是( )
| A. | 水银 | B. | 硝酸钾 | C. | 酒精 | D. | 蔗糖 |
15.下列离子方程式正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | |
| C. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2A1O2-+3H2↑ |
5.二氧化硫不具有的性质是( )
| A. | 无色无味 | B. | 漂白性 | C. | 还原性 | D. | 会形成酸雨 |
12.2SO2+O2?2SO3△H<0是工业上接触法制硫酸的重要反应.下列关于该反应的说法不正确的是( )
| A. | 增加O2的浓度提高SO2的转化率 | |
| B. | 利用该反应放出的热量对SO2、O2预热 | |
| C. | 降低温度能加快反应的速率 | |
| D. | 即使增大压强也不能使SO2全部转化为SO3 |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,18 g H20所含的中子数为10NA | |
| B. | 一定条件下1 mol铁粉与浓硫酸反应,转移电子数一定为3NA | |
| C. | 在1 L的碳酸钠溶液中,若c(CO32一)=1 mol•L-1,则Na+数目大于2NA | |
| D. | 含阴阳离子总数为4NA的固体Na202溶于水配成1 L溶液,所得溶液中Na+的物质的量浓度为2 mol•L-1 |

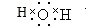
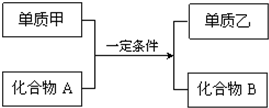 置换反应的通式可表示为:
置换反应的通式可表示为: