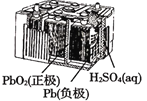
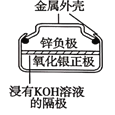
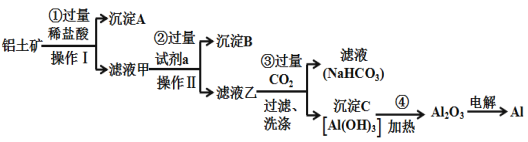
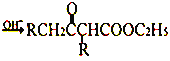题目内容
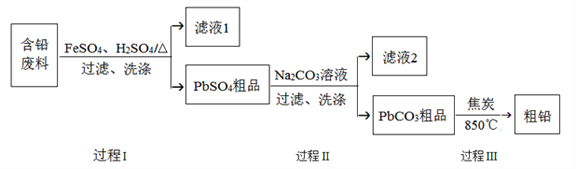
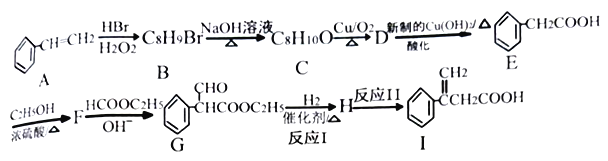
【题目】叶蝉散对水稻叶蝉和飞虱具有较强的触杀作用,防效迅速,但残效不长。工业上用邻异丙基苯酚合成叶蝉散的过程如下:
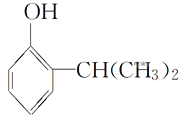 (邻异丙基苯酚)
(邻异丙基苯酚)![]()
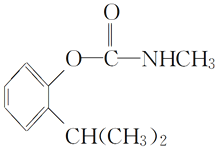 (叶蝉散)
(叶蝉散)
下列有关说法正确的是( )
A.叶蝉散的分子式是C11H16NO2B.邻异丙基苯酚的核磁共振氢谱有7个峰
C.叶蝉散分子中含有羧基D.邻异丙基苯酚与![]() 互为同系物
互为同系物
【答案】B
【解析】
A.根据叶蝉散的结构可以看出,分子中有11个C原子、15个H原子、1个N原子、2个O原子,故分子式为C11H15NO2,A错误;
B.邻异丙基苯酚有7种不同化学状态的H原子,故核磁共振氢谱中有7组峰,B正确;
C.根据叶蝉散的结构,分子中不含羧基,C错误;
D.邻异丙基苯酚(属于酚类)与![]() (属于醇类)的结构不同,故不属于同系物,D错误;
(属于醇类)的结构不同,故不属于同系物,D错误;
故选B。

 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案【题目】从能量的变化和反应的快慢等角度研究化学反应具有重要意义。
(1)已知一定条件下,反应N2+3H2![]() 2NH3为放热反应;:
2NH3为放热反应;:
①下图能正确表示该反应中能量变化的是________;
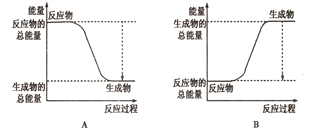
②根据下表数据,计算生成1molNH3时该反应放出的热量为______kJ;
化学键 | H-H | N≡N | N-H |
断开1mol键所吸收的能量 | 436kJ | 946kJ | 391kJ |
③一定温度下,将3molH2和1molN2通入容积为2L的密闭容器中发生反应,5min达到平衡,测得c(NH3)=0.4mol/L,则O至5min时![]() (N2)=______,反应开始与平衡时气体的物质的量之比为__________;
(N2)=______,反应开始与平衡时气体的物质的量之比为__________;
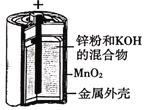
(2)原电池可将化学能转化为电能。由A、B、C、D四种金属按下表中装置进行实验:
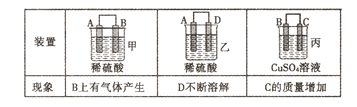
①装置甲甲SO42-向________ 极移动(填“A”或“B”);
②四种金属活动性由强到弱的顺序是____;
③若装置丙中的电极为质量相等的铁棒和铜棒,电池工作一段时间后.取出洗净、干燥、称量.两电极质量差为6g。则导线中通过电子的物质的量为______mol。