题目内容

为了鉴别上述化合物,分别完成以下实验:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B_________D__________。
(2)将含1 mol A的溶液与含1 mol E的溶液混合,所得溶液中所有离子的浓度由大到小的顺序是_______________________。
(3)写出实验②发生反应的离子方程式___________________。
(4)向含1mol C的溶液中滴加1000 mL 2 mol/L Ba(OH)2溶液,充分反应后溶液pH______7(填“大 于”、“小于”或“等于”),用离子方程式解释其原因_____________________。
(2)c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
(3)Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O
(4)大于;AlO2-+2H2O
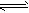 Al(OH)3+OH-
Al(OH)3+OH- 
已知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4。三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某化学兴趣小组通过实验来探究某红色粉末是Fe2O3或Cu2O或两者的混合物。(实验所需试剂只能从下列中选择:稀硫酸、KSCN溶液、稀硝酸、双氧水、铁粉、碱式碳酸铜)
探究方案:将红色粉末溶于足量的稀硫酸中;实验现象:反应后有红色固体存在;
(1)结论:红色粉末是 。
(2)如果红色粉末是Cu2O和少量Fe2O3的混合物,请设计实验证明之。
实验操作:
实验现象:
(3)兴趣小组欲利用Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知:在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀的pH | 6.4 | 9.7 | 1.9 |
| 沉淀完全的pH | 9.6 | 12.7 | 3.7 |
已知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4。三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某化学兴趣小组通过实验来探究某红色粉末是Fe2O3或Cu2O或两者的混合物。(实验所需试剂只能从下列中选择:稀硫酸、KSCN溶液、稀硝酸、双氧水、铁粉、碱式碳酸铜)
探究方案:将红色粉末溶于足量的稀硫酸中;实验现象:反应后有红色固体存在;
(1)结论:红色粉末是 。
(2)如果红色粉末是Cu2O和少量Fe2O3的混合物,请设计实验证明之。
实验操作:
实验现象:
(3)兴趣小组欲利用Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知:在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀的pH | 6.4 | 9.7 | 1.9 |
| 沉淀完全的pH | 9.6 | 12.7 | 3.7 |
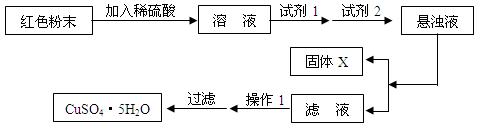
实验小组设计如下实验方案:
试回答:
①试剂1为 ,试剂2为 (填名称);
加入试剂1后发生反应的离子方程式为________________________,_______________________。
②固体X的化学式为 ;
③操作1为 。
已知:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4。三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某化学兴趣小组通过实验来探究某红色粉末是Fe2O3或Cu2O或两者的混合物。(实验所需试剂只能从下列中选择:稀硫酸、KSCN溶液、稀硝酸、双氧水、铁粉、碱式碳酸铜)
探究方案:将红色粉末溶于足量的稀硫酸中;实验现象:反应后有红色固体存在;
(1)结论:红色粉末是 。
(2)如果红色粉末是Cu2O和少量Fe2O3的混合物,请设计实验证明之。
实验操作:
实验现象:
(3)兴趣小组欲利用Fe2O3和Cu2O的混合物制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知:在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
|
物质 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
开始沉淀的pH |
6.4 |
9.7 |
1.9 |
|
沉淀完全的pH |
9.6 |
12.7 |
3.7 |
实验小组设计如下实验方案:
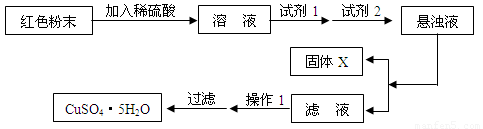
试回答:
①试剂1为 ,试剂2为 (填名称);
加入试剂1后发生反应的离子方程式为________________________,_______________________。
②固体X的化学式为 ;
③操作1为 。