题目内容
10.下列质的系统命名中,错误的是( )| A. | 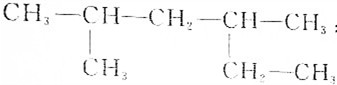 :2,4-二甲基已烷 :2,4-二甲基已烷 | |
| B. | 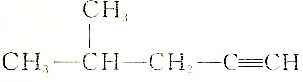 :2-甲基-4-戊炔 :2-甲基-4-戊炔 | |
| C. | 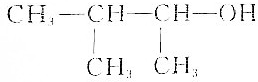 :3-甲基-2-丁醇 :3-甲基-2-丁醇 | |
| D. | CH2-CHBr-CHBr-CH3:2,3-二溴丁烷 |
分析 A、烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,据此分析;
B、炔烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
C、醇命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
D、卤代烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置.
解答 解:A、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,故为己烷,从离支链近的一端给主链上碳原子编号,故在2号和4号碳原子上各有一个甲基,故为2,4-二甲基己烷,故A正确;
B、炔烃命名时,要选含官能团的最长的碳链为主链,故为戊炔,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置,故在4号碳原子上有一个甲基,在1号和2号碳原子间存在碳碳三键,故名称为4-甲基-1-戊炔,故B错误;
C、醇命名时,要选含官能团的最长的碳链为主链,故为丁醇,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置,故在2号碳原子上有-OH,在3号碳原子上有一个甲基,故名称为3-甲基=2-丁醇,故C正确;
D、卤代烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,故在2号和3号上各有一个-Br,故名称为2,3-二溴丁烷,故D正确.
故选B.
点评 本题考查了烷烃、炔烃、醇和卤代烃的命名,难度不大,应注意的是含官能团的有机物在命名时,要以官能团为考虑对象来选主链和编号位.

练习册系列答案
相关题目
20.锶(Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素.用天青石(主要成分为SrSO4,含有少量BaCO3、FeO、Fe2O3、Al2O3、SiO2等)制备SrCO3,工艺流程如图1:
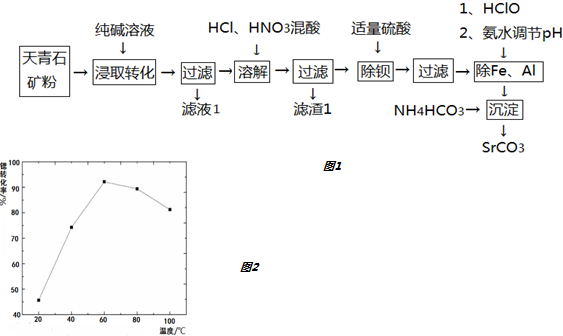
已知:
(1)“浸取转化”过程中发生的化学方程式为:SrSO4+Na2CO3=SrCO3+Na2SO4;当转化完全时,混合液中的c(CO32-)=1.0×10-3 mol•L-1,则c(SO42-)=2.0mol/L.
(2)滤液1的主要成分为Na2SO4或硫酸钠;滤渣1的主要成分为SiO2.
(3)“除钡”过程中硫酸不要过量,原因是硫酸过量后会生成SrSO4沉淀,降低产率.
(4)“沉淀”生成SrCO3的离子方程式为Sr2++2HCO3-=SrCO3↓+H2O+CO2↑.
沉淀过程中,温度对Sr2+生成SrCO3反应转化率的影响见如图2,60℃之前,锶转化率随温度升高而变大的主要原因是升温有利于CO2的逸出
(5)以SrCO3粉作原料经高温焙烧分解成SrO,再将SrO与铝粉充分混合并压制,真空环境下通过热还原反应可制得金属Sr,同时获得3SrO•Al2O3渣团.请写出热还原反应的化学方程式6SrO+2Al$\frac{\underline{\;\;△\;\;}}{\;}$3Sr+3SrO•Al2O3.

已知:
| SrSO4 | BaSO4 | SrCO3 | |
| Ksp | 3.2×10-7 | 1.1×10-10 | 1.6×10-10 |
(2)滤液1的主要成分为Na2SO4或硫酸钠;滤渣1的主要成分为SiO2.
(3)“除钡”过程中硫酸不要过量,原因是硫酸过量后会生成SrSO4沉淀,降低产率.
(4)“沉淀”生成SrCO3的离子方程式为Sr2++2HCO3-=SrCO3↓+H2O+CO2↑.
沉淀过程中,温度对Sr2+生成SrCO3反应转化率的影响见如图2,60℃之前,锶转化率随温度升高而变大的主要原因是升温有利于CO2的逸出
(5)以SrCO3粉作原料经高温焙烧分解成SrO,再将SrO与铝粉充分混合并压制,真空环境下通过热还原反应可制得金属Sr,同时获得3SrO•Al2O3渣团.请写出热还原反应的化学方程式6SrO+2Al$\frac{\underline{\;\;△\;\;}}{\;}$3Sr+3SrO•Al2O3.
1.化学与生产、生活、社会密切相关,下列有关说法中正确的是( )
| A. | 苯酚有一定毒性,不能作消毒剂和防腐剂 | |
| B. | 纤维素可水解成葡萄糖,人类可从中获得生存所需的能量 | |
| C. | 2014年1月,国家首次将雾霾天气纳入自然灾情进行通报,雾霾是一种不同于胶体的分散系,它的形成与大量焚烧田间秸秆有关 | |
| D. | 煤经气化和液化两个物理变化过程,可变为清洁能源 |
18.如表为元素周期表的一部分,X、Y、Z、W为短周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍,下列说法正确的是( )
| X | Y | ||
| Z | W | ||
| T |
| A. | 根据元素周期律,可以推测存在T3Y4、TZ2和TW4 | |
| B. | X氢化物的沸点一定比Y氢化物的沸点低 | |
| C. | XZ2、XW4与YW3都是非极性分子 | |
| D. | W的氧化物的水化物酸性一定比Z的强 |
15.在国际环境问题中,一次性使用聚苯乙烯材料带来的“白色污染”极为严重.这种材料难分解,处理麻烦.最近研制出了一种新材料: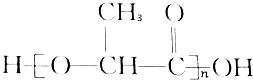 能代替聚苯乙烯,它是由乳酸缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )
能代替聚苯乙烯,它是由乳酸缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )
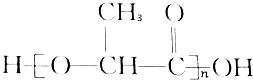 能代替聚苯乙烯,它是由乳酸缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )
能代替聚苯乙烯,它是由乳酸缩聚而成,能在乳酸菌的作用下降解而消除对环境的污染.下列关于聚乳酸的说法正确的是( )| A. | 聚乳酸是一种纯净物 | B. | 聚乳酸的单体是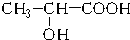 | ||
| C. | 聚乳酸是一种羧酸 | D. | 其聚合方式和乙烯相同 |
5.《化学反应原理》一书中,我们学习了两个重要的定量实验.请回答下列问题:
Ⅰ、某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
已知:Q(放)=C m(t2-t1),反应后溶液的比热容C为4.18KJ?℃-1?Kg-1,m指溶液的质量,各物质的密度均为1g?cm-3.
①计算分析△H=-56.8KJ/mol.(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8KJ/mol.
Ⅱ、为了测定含有H2C2O4•2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液.
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/L NaOH溶液滴定,消耗NaOH溶液20.00mL.
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL.
回答下列问题:
(1)已知:0.10mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为c(HC2O4-)>c(C2O42-)>c(H2C2O4).
(2)完成并配平下列离子方程式
5C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O.
(3)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4•2H2O的质量分数偏小.(填“偏大”、“偏小”或“无影响”)
(4)步骤③中判断滴定终点的方法是滴入最后一滴溶液呈紫红色且半分钟颜色不变.
(5)常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
(i)写出H2C2O4的电离方程式H2C2O4?H++HC2O4-,HC2O4-?H++C2O42-.
(ii)KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题)HC2O4-?H++C2O42-,HC2O4-+H2O?H2C2O4+OH-,但其电离程度大于水解程.
(iii)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42- ) b.c(Na+)═c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42- ) d.c(K+)>c(Na+)
Ⅰ、某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、5mol?L-1 盐酸、0.55mol?L-1NaOH溶液,尚缺少的实验玻璃用品是量筒、温度计.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?否(填“能”或“否”),其原因是金属易导热,热量散失导致误差大.
(3)他们记录的实验数据如下:
| 实 验 试剂如下: | 溶 液 温 度 | 中和热△H | ||||
| t1 | t2 | |||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | ||
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | ||
①计算分析△H=-56.8KJ/mol.(结果保留3位有效数字)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8KJ/mol.
Ⅱ、为了测定含有H2C2O4•2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液.
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/L NaOH溶液滴定,消耗NaOH溶液20.00mL.
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL.
回答下列问题:
(1)已知:0.10mol/L KHC2O4溶液pH约为3,其中含碳元素的粒子浓度由大到小的顺序为c(HC2O4-)>c(C2O42-)>c(H2C2O4).
(2)完成并配平下列离子方程式
5C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O.
(3)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得的H2C2O4•2H2O的质量分数偏小.(填“偏大”、“偏小”或“无影响”)
(4)步骤③中判断滴定终点的方法是滴入最后一滴溶液呈紫红色且半分钟颜色不变.
(5)常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示:
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(ii)KHC2O4溶液显酸性的原因是 (请用方程式并结合必要的文字回答该小题)HC2O4-?H++C2O42-,HC2O4-+H2O?H2C2O4+OH-,但其电离程度大于水解程.
(iii)向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)═c(HC2O4-)+c(H2C2O4)+c(C2O42- ) b.c(Na+)═c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)═c(HC2O4-)+c(C2O42- ) d.c(K+)>c(Na+)
2.要除去氯化亚铁溶液中的少量氯化铁,可行的办法是( )
| A. | 滴入KSCN溶液 | B. | 通入氯气 | C. | 滴入NaOH溶液 | D. | 加入铁粉 |
3.下列有关“化学与生活、社会”的叙述正确的是( )
| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| C. | 药皂中含有苯酚,能杀菌消毒,故苯酚具有强氧化性 | |
| D. | 屠呦呦获得了2015年诺贝尔奖,她用乙醚提取青蒿素的过程属于化学变化 |