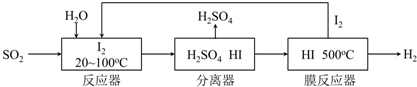
题目内容
3.下列有关“化学与生活、社会”的叙述正确的是( )| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| C. | 药皂中含有苯酚,能杀菌消毒,故苯酚具有强氧化性 | |
| D. | 屠呦呦获得了2015年诺贝尔奖,她用乙醚提取青蒿素的过程属于化学变化 |
分析 A.气溶胶为胶体分散系;
B.碘是人体必须微量元素,每人每天大约吃食盐12克,多吃无益;
C.苯酚无强氧化性;
D.乙醚提取青蒿素无新物质生成.
解答 解:A.气溶胶为胶体分散系,有丁达尔效应,故A正确;
B.碘是人体必需微量元素,所以要吃富含KIO3的食盐,但不能多吃,多吃会导致升高血压,促进动脉粥样硬化,故B错误;
C.苯酚的水溶液可使菌体蛋白变性杀菌消毒,但苯酚无强氧化性,故C错误;
D.乙醚提取青蒿素无新物质生成,属于物理变化,故D错误;
故选:A.
点评 本题考查较为综合,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养,提高学生学习的积极性,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
10.下列质的系统命名中,错误的是( )
| A. | 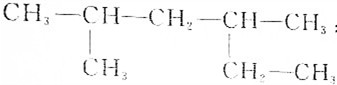 :2,4-二甲基已烷 :2,4-二甲基已烷 | |
| B. | 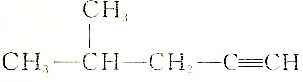 :2-甲基-4-戊炔 :2-甲基-4-戊炔 | |
| C. | 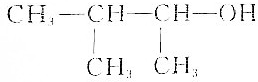 :3-甲基-2-丁醇 :3-甲基-2-丁醇 | |
| D. | CH2-CHBr-CHBr-CH3:2,3-二溴丁烷 |
14.Al-H2O2电池是一种新型的高性能电源,其结构如图所示.下列说法错误的是( )
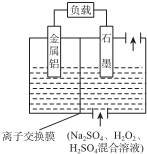

| A. | 铝作该电源的负极,电极反应为:Al-3e-═Al3+ | |
| B. | 电池总反应:2Al+3H2O2+6H+═2Al3++6H2O | |
| C. | 放电时溶液中的SO42-向正极移动 | |
| D. | 放电时正极周围溶液的pH升高 |
11.阿托酸是一种常用的医药中间体,其结构如图所示: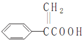 .下列有关说法中错误的是( )
.下列有关说法中错误的是( )
 .下列有关说法中错误的是( )
.下列有关说法中错误的是( )| A. | 溴单质能与阿托酸发生加成反应 | |
| B. | 阿托酸能与硝酸发生取代反应 | |
| C. | 可用酸性KMnO4溶液区别阿托酸与苯 | |
| D. | 阿托酸分子中含有4个碳双键 |
15.下列实验不能达到预期目的是( )
| A. | 用稀硫酸和锌粒反应制取氢气时加入少许硫酸铜粉末以加快反应速率 | |
| B. | 向乙酸乙酯中加入饱和碳酸钠溶液以除去乙酸乙酯中少量的乙酸 | |
| C. | 向盛有沸水的烧杯中滴加FeC13饱和溶液并长时间煮沸以制取Fe(OH)3胶体 | |
| D. | 向蔗糖中滴加浓硫酸可证明浓硫酸有脱水性 |
12.胡妥油(D)用作香料的原料,它可由A合成得到:
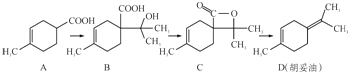
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 若有机物A是由异戊二烯(C5H8)和丙烯酸(C3H4O2)加热得到的,则该反应的反应类型属于加成反应 | |
| B. | 有机物B既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体 | |
| C. | 有机物C的所有同分异构体中不可能有芳香族化合物存在 | |
| D. | 有机物D能发生加成、取代、氧化、还原等反应 |
13.下列关于物质分类的说法正确的是( )
| A. | NaH、NH3都属于共价化合物 | B. | 12C、C60都属于碳的同素异形体 | ||
| C. | 水玻璃、硅酸都属于胶体 | D. | 生铁、青铜都属于合金 |