题目内容
3.下列说法正确的是( )| A. | 用如图装置除去乙烷中混有的乙烯 | |
| B. | 配制一定物质的量浓度的溶液,定容时仰视刻度,溶液浓度偏大 | |
| C. | 制备乙酸乙酯时,将乙醇和乙酸依次加入浓硫酸中 | |
| D. | 玻璃仪器洗涤干净的标准是:附着在仪器内壁上的水既不聚集成滴,也不成股流下 |
分析 A.高锰酸钾能将乙烯氧化为二氧化碳;
B.仰视刻度线,会导致加入的蒸馏水体积偏大,配制的溶液浓度偏低;
C.制取混合酸时,需要类比浓硫酸的稀释进行操作,应该将浓硫酸加入到乙醇中;
D.当玻璃仪器附着在仪器内壁上的水既不聚集成滴,也不成股流下时,可说明洗涤干净.
解答 解:A.高锰酸钾能将乙烯氧化为二氧化碳混于乙烷中成为新的杂质,故A错误;
B.配制一定物质的量浓度的溶液,定容时仰视刻度,会导致加入的蒸馏水体积偏大,配制的溶液浓度偏低,故B错误;
C.浓硫酸溶于水放出大量的热,且密度比水大,为防止酸液飞溅,应先在烧瓶中加入一定量的乙醇,然后慢慢将浓硫酸加入烧瓶,边加边振荡,不能先加入浓硫酸再加入乙醇,故C错误;
D.当玻璃仪器附着在仪器内壁上的水既不聚集成滴,也不成股流下时,可说明洗涤干净,故D正确.
故选D.
点评 本题考查较为综合,涉及物质的制备、分离、提纯以及溶液配制等,为高频考点,侧重于学生的分析能力和实验能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
5.下列叙述正确的是( )
| A. | 价电子排布为4s24p2的元素位于第四周期第ⅤA族,是P区元素 | |
| B. | 1,2-二甲苯核磁共振氢谱中有三组峰,且氢原子数之比为3:1:1 | |
| C. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 | |
| D. | 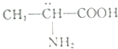 分子属于手性分子 分子属于手性分子 |
14.通常用来衡量一个国家的石油化学工业发展水平的标志是( )
| A. | 石油的年产量 | B. | 硫酸的年产量 | ||
| C. | 合成纤维的年产量 | D. | 乙烯的年产量 |
18.常温下,下列叙述中不正确的是( )
| A. | NH4HSO4溶液中离子浓度大小关系:c(H+)>c(SO42-)>c(NH4+)>c(OH-) | |
| B. | 等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和,则a+b=14 | |
| C. | Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| D. | NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
15.实验室常用亚硫酸钠固体和70%的浓硫酸制备SO2气体,反应方程式为Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,请设计一套实验装置,收集一试管干燥的SO2气体.
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:
(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)
(3)某实验小组用如图乙装置测定收集到的气体中SO2的含量,反应管中装有酸性高猛酸钾溶液.
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量偏低(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积).用c、V1、V2表示SO2的体积百分含量为=$\frac{56{V}_{1}c}{56{V}_{1}c+V{\;}_{2}}$×100%.
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:

(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)
| 仪器标号 | 仪器中所加物质 | 作用 |
| A | 亚硫酸钠、浓硫酸 | 产生SO2 |
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量偏低(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积).用c、V1、V2表示SO2的体积百分含量为=$\frac{56{V}_{1}c}{56{V}_{1}c+V{\;}_{2}}$×100%.
12.下列试剂不会因为空气的氧气而变质的是( )
| A. | 硅酸钠溶液 | B. | 硫酸亚铁溶液 | C. | 亚硫酸钠溶液 | D. | 氢硫酸 |
13.下列离子方程式正确的是( )
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 二氧化硫通入次氯酸钠溶液:SO2+ClO-+OH-=SO42-+Cl-+H2O | |
| C. | 硫酸工业尾气中的SO2用过量的氨水吸收:2NH3•H2O+SO2=2NH4++SO32-+H2O | |
| D. | Cu溶于浓HNO3:Cu+4H++2NO3-=Cu2++2NO↑+4H2O |
 甲、乙、丙是三种常见单质,A、B、C是常见化合物,B在常温下为液态.在一定条件下上述物质之间的关系如图.
甲、乙、丙是三种常见单质,A、B、C是常见化合物,B在常温下为液态.在一定条件下上述物质之间的关系如图. 氧化-还原反应是中学化学中一类重要的反应类型,在日常生活中很常见,请回答:(1)在反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中.当产生标况下4.48L气体时,消耗单质铜19.2g,此时转移了0.6mol电子.
氧化-还原反应是中学化学中一类重要的反应类型,在日常生活中很常见,请回答:(1)在反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中.当产生标况下4.48L气体时,消耗单质铜19.2g,此时转移了0.6mol电子.