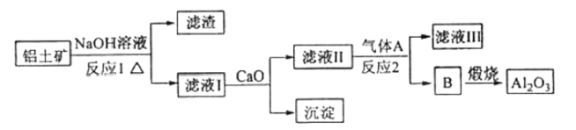
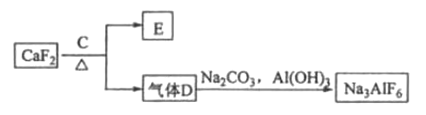
题目内容
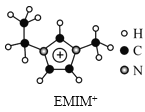
【题目】离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
(1)碳原子价层电子的轨道表达式为__,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为__形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是__。NH3比PH3的沸点高,原因是__。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是__。
(4)EMIM+离子中,碳原子的杂化轨道类型为__。分子中的大π键可用符号Π![]() 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为Π![]() ),则EMIM+离子中的大π键应表示为__。
),则EMIM+离子中的大π键应表示为__。
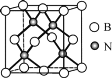
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于__晶体,其中硼原子的配位数为__。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为__(列出化简后的计算式)。
【答案】![]() 哑铃 NH3 氨分子间存在氢键 基态氮原子电子占据的最高能级为半充满,较稳定 sp2、sp3 Π
哑铃 NH3 氨分子间存在氢键 基态氮原子电子占据的最高能级为半充满,较稳定 sp2、sp3 Π![]() 原子 4
原子 4 ![]()
【解析】
根据核外电子排布原则确定电子排布图,根据价层电子对互斥理论计算价层电子对数,根据第一电离能的规律比较第一电离能,根据轨道杂化理论确定杂化轨道类型,根据大π键形成的原理确定大π键的表示,根据晶体知识确定晶胞类型、配位数及空间占有率。
(1)碳原子价电子数为4,价电子排布式为2s22p2,所以价层电子的轨道表达式为![]() ;基态碳原子核外电子占据的最高能级为2p,2p轨道的电子云轮廓图为哑铃形;
;基态碳原子核外电子占据的最高能级为2p,2p轨道的电子云轮廓图为哑铃形;
(2)NH3中N原子价层电子对数为![]() ,
,
![]() 中N原子价层电子对数
中N原子价层电子对数![]() ,
,
![]() 中N原子价层电子对数
中N原子价层电子对数![]() ,所以中心原子价层电子对数不同于其他其他两种粒子的是NH3; NH3比PH3的沸点高是因为NH3分子间存在氢键,而PH3分子间只有范德华力;
,所以中心原子价层电子对数不同于其他其他两种粒子的是NH3; NH3比PH3的沸点高是因为NH3分子间存在氢键,而PH3分子间只有范德华力;
(3)第VA族比同周期相邻元素都大,是因为最高能级p轨道上电子数为特殊的半充满状态,能量低、较稳定,所以氮元素的第一电离能比同周期相邻元素都大的原因是基态氮原子电子占据的最高能级为半充满,较稳定;
(4)根据图中EMIM+离子中键总数为5个,根据图像,EMIM+离子中C原子的空间构型有四面体和平面三角形两种,即C原子采用sp3、sp2杂化;EMIM+离子有6个电子可形成大π键,形成的大π键原子数为5,故可用符号Π![]() 表示;
表示;
(5)立方氮化硼硬度仅次于金刚石,晶体类型类似于金刚石,是原子晶体;晶胞中每个N原子连接4个B原子,氮化硼化学式BN,所以晶胞中每个B原子也连接4个N原子,即硼原子的配位数为4;晶胞中N原子数为4, B原子数![]() ,晶胞质量为
,晶胞质量为![]() ,晶胞体积为
,晶胞体积为 ,B、N原子的总体积为
,B、N原子的总体积为![]() ,晶胞中原子的空间利用率为
,晶胞中原子的空间利用率为 ;
;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】碳及其化合物广泛存在于自然界。请回答下列问题:
(1)反应Ⅰ:![]() △H1 平衡常数为K1
△H1 平衡常数为K1
反应Ⅱ:![]() △H2 平衡常数为K2
△H2 平衡常数为K2
不同温度下,K1、K2的值如下表:
| K1 | K2 |
973 | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
现有反应Ⅲ:![]() ,结合上表数据,反应Ⅲ是________(填“放热”或“吸热”)反应。
,结合上表数据,反应Ⅲ是________(填“放热”或“吸热”)反应。
(2)![]() 催化加氢合成二甲醚是一种
催化加氢合成二甲醚是一种![]() 转化方法,其过程中主要发生下列反应:
转化方法,其过程中主要发生下列反应:
反应Ⅲ:![]() △H3
△H3
反应Ⅳ:![]() △H=-122.5kJ/mol
△H=-122.5kJ/mol
在恒压、![]() 和
和![]() 的起始量一定的条件下,
的起始量一定的条件下,![]() 平衡转化率和平衡时
平衡转化率和平衡时![]() 的选择性随温度的变化如图。
的选择性随温度的变化如图。
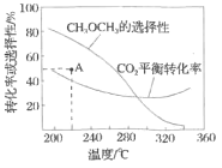
其中:![]() 的选择性
的选择性![]()
①温度高于300℃,![]() 平衡转化率随温度升高而上升的原因是________。
平衡转化率随温度升高而上升的原因是________。
②220℃时,在催化剂作用下![]() 与
与![]() 反应一段时间后,测得
反应一段时间后,测得![]() 的选择性为48%(图中
的选择性为48%(图中![]() 点)。不改变反应时间和温度,一定能提高
点)。不改变反应时间和温度,一定能提高![]() 选择性的措施有________。
选择性的措施有________。
(3)石油化工生产中,利用裂解反应可以获得重要化工原料乙烯、丙烯。一定条件下,正丁烷裂解的主反应如下:
反应Ⅴ:![]()
反应Ⅵ:![]()
一定温度下,向容积为![]() 的密闭容器中通入正丁烷,反应时间
的密闭容器中通入正丁烷,反应时间![]() 与容器内气体总压强
与容器内气体总压强![]() 数据如下:
数据如下:
| 0 | 10 | 20 | 30 | 40 |
| 5 | 7.2 | 8.4 | 8.8 | 8.8 |
①反应速率可以用单位时间内分压的变化表示,即v=![]() ,前
,前![]() 内正丁烷的平均反应速率v(正丁烷)
内正丁烷的平均反应速率v(正丁烷)![]() ________
________![]() ,该温度下,正丁烷的平衡转化率
,该温度下,正丁烷的平衡转化率![]() ________。
________。
②若平衡时乙烯的体积分数为![]() ,则该温度下反应Ⅴ的分压平衡常数Kp=________MPa(保留一位小数)。
,则该温度下反应Ⅴ的分压平衡常数Kp=________MPa(保留一位小数)。
③若反应在恒温、恒压条件下进行,平衡后反应容器的体积________![]() (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。