题目内容
等质量的CuO和MgO粉末分别溶于相同体积的硝酸中,得到Cu(NO3)2和Mg(NO3)2溶液的浓度分别为amol/L和bmol/L,用等式表示 a与b的关系 .
考点:化学方程式的有关计算
专题:计算题
分析:设它们的质量都是80g,则利用n=
来计算物质的量,再由原子守恒来分析Cu(NO3)2和Mg(NO3)2的物质的量,因溶液体积相同,则溶质的物质的量的比值等于浓度之比.
| m |
| M |
解答:
解:设CuO和MgO粉末的质量均为80g,
则n(CuO)=
=1mol,
n(MgO)=
=2mol,
由原子守恒可知,则n[Cu(NO3)2]=n(CuO)=1mol,n[Mg(NO3)2]=n(MgO)=2mol
因溶液体积相同,则溶质的物质的量的比值等于浓度之比,故a:b=1mol:2mol=1:2,即2a=b,
故答案为:2a=b.
则n(CuO)=
| 80g |
| 80g/mol |
n(MgO)=
| 80g |
| 40g/mol |
由原子守恒可知,则n[Cu(NO3)2]=n(CuO)=1mol,n[Mg(NO3)2]=n(MgO)=2mol
因溶液体积相同,则溶质的物质的量的比值等于浓度之比,故a:b=1mol:2mol=1:2,即2a=b,
故答案为:2a=b.
点评:本题考查物质的量浓度计算,难度不大,旨在考查学生对常用化学计量的理解,注意利用原子守恒解答.

练习册系列答案
相关题目
下列各溶液中,一定能大量共存的是( )
| A、Fe2+、Na+、SO42-、H2O2 |
| B、CH3CHO、MnO4-、H+、K+ |
| C、Pb2+、K+、SO42-、Cl- |
| D、Na+、SO32-、CH3COO-、S2- |
过氧化氢被称为绿色氧化剂,下列叙述中不正确的是( )
| A、在H2O2分子中含有O22- |
| B、纯H2O2能与水以任意比例混合成H2O2的水溶液 |
| C、H2O2常用作消毒剂 |
| D、在酸性溶液中,H2O2是强氧化剂,还原性较弱 |
某固体物质A在一定条件下受热分解产物都是气体,有关的化学方程式为:2A═B↑+2C↑+2D↑.若生成的混合气体对氘气的相对密度为d,则A的相对分子质量为( )
| A、2d | B、2.5d |
| C、5d | D、10d |
下列化学表达方式不正确的是( )
| A、中子数为20的氯原子:37Cl |
B、Cl-的结构示意图 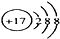 |
C、氢氧根离子的电子式: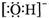 |
| D、HClO的结构式 H-Cl-O |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol N2所含有的原子数为NA |
| B、标准状况下,22.4 L水中含有的水分子数为NA |
| C、标准状况下,22.4 L氯化氢所含的原子数为NA |
| D、32 g O2分子和32 g O3分子所含的氧原子数目相等 |
 在试管中加入一定量的盐酸和Al条,H2体积随时间变化的图象如图,该实验结果中能说明“温度越高,反应速率越快”的事实是
在试管中加入一定量的盐酸和Al条,H2体积随时间变化的图象如图,该实验结果中能说明“温度越高,反应速率越快”的事实是