题目内容
下列化学表达方式不正确的是( )
| A、中子数为20的氯原子:37Cl |
B、Cl-的结构示意图 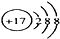 |
C、氢氧根离子的电子式: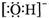 |
| D、HClO的结构式 H-Cl-O |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氯原子的核电荷数为17,元素符号的左上角表示的是质量数,质量数=质子数+中子数;
B.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构;
C.氢氧根离子为阴离子,电子式中需要标出所带电荷及原子的最外层电子;
D.次氯酸中存在1个氧氯将和一个氧氢键,不存在氢氯键.
B.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构;
C.氢氧根离子为阴离子,电子式中需要标出所带电荷及原子的最外层电子;
D.次氯酸中存在1个氧氯将和一个氧氢键,不存在氢氯键.
解答:
解:A.氯元素质子数为17,中子数为20的氯原子的质量数为37,该原子可以表示为:37Cl,故A正确;
B.氯离子的核电荷数为17、核外电子总数为18,Cl-的结构示意图为: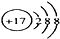 ,故B正确;
,故B正确;
C.氢氧根离子为阴离子,氧原子最外层达到8个电子,氢氧根离子的电子式为: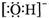 ,故C正确;
,故C正确;
D.次氯酸的电子式为: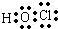 ,将所有共用电子对换成短线即为结构式,次氯酸正确的结构式为:H-O-Cl,故D错误;
,将所有共用电子对换成短线即为结构式,次氯酸正确的结构式为:H-O-Cl,故D错误;
故选D.
B.氯离子的核电荷数为17、核外电子总数为18,Cl-的结构示意图为:
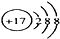 ,故B正确;
,故B正确;C.氢氧根离子为阴离子,氧原子最外层达到8个电子,氢氧根离子的电子式为:
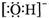 ,故C正确;
,故C正确;D.次氯酸的电子式为:
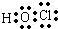 ,将所有共用电子对换成短线即为结构式,次氯酸正确的结构式为:H-O-Cl,故D错误;
,将所有共用电子对换成短线即为结构式,次氯酸正确的结构式为:H-O-Cl,故D错误;故选D.
点评:本题考查了常见化学用语的书写判断,题目难度中等,注意掌握原子结构示意图、电子式、结构式、元素符号的概念及表示方法,选项D为易错点,注意次氯酸中存在氢氯键.

练习册系列答案
相关题目
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e=ZnO+H2O,Ag2O+H2O+2e=2Ag+2OH-,总反应为:Ag2O+Zn=2Ag+ZnO 根据上述反应式,判断下列叙述中,正确的是( )
| A、在使用过程中,电池负极区溶液pH值增大 |
| B、在使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C、Zn是负极,Ag2O是正极 |
| D、Zn电极发生还原反应,Ag2O电极发生氧化反应 |
在1LNa2SO4的Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol/L,加入1L0.3mol/L的BaCl2溶液恰好使SO42-完全沉淀,则混合容易中Na+的浓度为( )
| A、0.3mol/L |
| B、0.45mol/L |
| C、0.6mol/L |
| D、0.15mol/L |
下列化学用语中,书写错误的是( )
A、硫离子的结构示意图: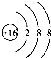 |
| B、次氯酸的结构式:H-O-Cl |
C、CO2的比例模型: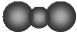 |
D、丙烷的球棍模型: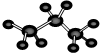 |
如图是常见四种有机物的比例模型示意图.下列说法正确的是( )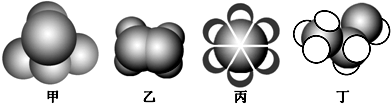

| A、甲能使酸性高锰酸钾溶液褪色 |
| B、乙可与溴水发生加成反应使溴水褪色 |
| C、丙中的碳碳键是碳碳单键和碳碳双键交替结合 |
| D、丁在稀硫酸作用下可与乙酸发生取代反应 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温常压下,14 g CO中含有的原子数目为NA |
| B、标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2 NA |
| C、25℃时,pH=13的1.0 L的Ba(OH)2溶液中含有的OH-数目为0.2 NA |
| D、1L1mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
下列电离方程式正确的是( )
| A、NaHCO3═Na++H++CO32- |
| B、NaHSO4═Na++H++SO42- |
| C、H2SO4═2H++SO4- |
| D、KClO3═K++Cl-+3O2- |
下列各组离子能大量共存的是( )
| A、I-、ClO-、H+、Na+ |
| B、K+、HCO3-、OH-、NH4+ |
| C、Fe3+、Cu2+、SO42-、Cl- |
| D、Ca2+、Na+、SO42-、SO32- |