题目内容
已知下列热化学方程式:
①C(s)+O2(g) CO2(g)△H=-393.5kJ/mol
②2CO(g)+O2(g) 2CO2(g)△H=-566.0kJ/mol
③N2(g)+2O2(g) 2NO2(g)△H=+68.0kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)1mol C(s) 完全燃烧生成CO2,放出的热量为
(3)CO的燃烧热△H=
①C(s)+O2(g) CO2(g)△H=-393.5kJ/mol
②2CO(g)+O2(g) 2CO2(g)△H=-566.0kJ/mol
③N2(g)+2O2(g) 2NO2(g)△H=+68.0kJ/mol
请回答:
(1)上述反应中属于放热反应的是
①②
①②
(填序号,下同),属于吸热反应的是③
③
.(2)1mol C(s) 完全燃烧生成CO2,放出的热量为
393.5
393.5
kJ.(3)CO的燃烧热△H=
-283.0
-283.0
kJ/mol.分析:(1)吸热为正放热为负;
(2)根据方程式①的△H解题;
(3)在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热.单位为kJ/mol;
(2)根据方程式①的△H解题;
(3)在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热.单位为kJ/mol;
解答:解:(1)在热化学方程式中吸热为正放热为负,属于放热反应的是①②;属于吸热反应的是③,故答案为:①②;③;
(2)根据方程式①的△H=-393.5kJ/mol,放出的热量为393.5kJ,故答案为:393.5;
(3)依据热化学方程式②:可得CO(g)+
O2(g)=CO2(g)△H=-283KJ/mol,故答案为:-283.0;
(2)根据方程式①的△H=-393.5kJ/mol,放出的热量为393.5kJ,故答案为:393.5;
(3)依据热化学方程式②:可得CO(g)+
| 1 |
| 2 |
点评:本题考查热化学方程式的意义、燃烧热的定义等,难度不大,注意燃烧热是指在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量.

练习册系列答案
相关题目
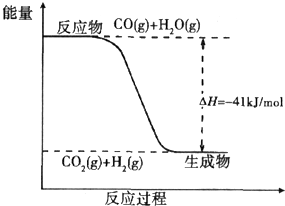 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.