题目内容
19.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.则下列说法不正确的是( )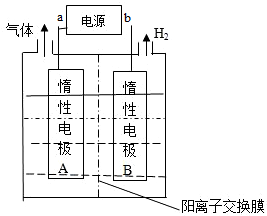
| A. | 外加电源的a极为正极 | |
| B. | 电解过程中,Li+向B极迁移 | |
| C. | 阳极反应式为:4OH--4e-═O2↑+H2O | |
| D. | 每生成1molLiOH,外电路转移1mol电子 |
分析 电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液,由图可知,右侧生成氢气,则B中氢离子放电,可知B为阴极,在B中制备LiOH,Li+由A经过阳离子交换膜向B移动;A中为LiCl溶液,氯离子放电生成氯气,据此回答.
解答 解:A、电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液,由图可知,右侧生成氢气,则B中氢离子放电,可知B为阴极,A为阳极,a是正极,故A正确;
B、电解过程中Li+向阴极即向B电极迁移,故B正确;
C、电解池的阳极上是氯离子失电子,电极反应式为:2Cl--2e-═Cl2↑,故C错误;
D、电解制备LiOH,B为阴极,在B中制备LiOH,每生成1molLiOH,外电路转移电子是1mol,故D正确;
故选C.
点评 本题是一道高考题的改编题,侧重电解原理的应用知识,注意知识的迁移和应用是解题的关键,难度中等.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
7.为了测量KI与K2S2O8反应的化学反应速率,某探究性学习小组,在不同条件下将10mol 0.12mol•L-1KI溶液(含少量淀粉)、10mol 0.10mol•L-1Na2S2O3溶液、20mol 0.06mol•L-1K2S2O8溶液混合进行实验,反应的离子方程式如下:2I-+S2O82-═I2+2SO42- I2+2S2O32-═2I-+S4O62-反应速率可以用溶液显蓝色时间t来度量.得到的时间数据如表所示(单位s),下列说法正确的是( )
| 温度 | pH=7 | pH=6 | pH=5 | pH=3 |
| 20℃ | 300 | 240 | 160 | 58 |
| 30℃ | 160 | 108 | 40 | 20 |
| 50℃ | 80 | 50 | x | 8 |
| A. | x可能为42 | |
| B. | 其他条件不变,在30°、pH=4下的反应速度比40℃、pH=6时快 | |
| C. | 根据单一变量法,无法比较温度、pH均不同的两组实验的反应速率较慢 | |
| D. | 30℃,pH=3条件下,KI的反应速率为v(KI)=0.005mol•L-1•s-1 |
14.CuSO4、Fe2(SO4)3的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol•L-1,则此溶液最多溶解铁粉的质量为( )
| A. | 5.6 g | B. | 11.2 g | C. | 22.4 g | D. | 20.16 g |
4. 结合如表回答下列问题(均为25℃时的数据)
结合如表回答下列问题(均为25℃时的数据)
(1)上述五种酸中,酸性最强的是HNO2 (填化学式).HCO3-的电离平衡常数表达式K=$\frac{c(C{{O}_{3}}^{2-})•c({H}^{+})}{c(HC{{O}_{3}}^{-})}$.
(2)已知硼酸(H3BO3)与足量NaOH溶液发生酸碱中和反应的离子方程式为:H3BO3+OH-=B(OH)4-,则硼酸为一元酸,硼酸的电离方程式为H3BO3+H2O?B(OH)4-+H+.
(3)常温下,0.01mol•L-1的HNO2 溶液加水稀释的过程中,下列各项数据增大的是④⑤(填代号).
①c(H+ ) ②$\frac{c(N{O}_{2}^{-})}{c({H}^{+})}$ ③Ka(HNO2)
④$\frac{c({H}^{+})}{c(HN{O}_{2})}$ ⑤c(OH-) ⑥$\frac{c(N{O}_{2}^{-})}{c(HN{O}_{2})•c(O{H}^{-})}$
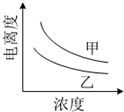
(4)如图描述的是醋酸与HNO2 在水中的电离度与浓度关系,
其中反映醋酸的是曲线乙 (填“甲”或“乙”,已知:电离度=已电离的溶质分子数/原有溶质分子总数).
(5)根据表中提供的数据可知,在溶液中能大量共存的微粒组是d (填代号).
a.H2CO3、HCO${\;}_{3}^{-}$、CH3COO-、CN- b.HCO${\;}_{3}^{-}$、CH3COOH、CN-、CO${\;}_{3}^{2-}$
c.HCN、HCO${\;}_{3}^{-}$、CN-、CO${\;}_{3}^{2-}$ d.HCN、HCO${\;}_{3}^{-}$、CH3COO-、CN
(6)设计一个现象明显、操作简便的实验方案证明HNO2酸性强于碳酸(不用叙述仪器和具体操作).
 结合如表回答下列问题(均为25℃时的数据)
结合如表回答下列问题(均为25℃时的数据)| 酸 | 电力平衡常数(Ka) | 酸 | 电力平衡常数(Ka) |
| CH3COOH | 1.7×10-5 | H3BO3 | 5.8×10-10 |
| H2CO3 | Ka1=4.2×10-7 Ka2=5.6×10-11 | HNO2 | 7.1×10-4 |
| HCN | 6.2×10-10 |
(2)已知硼酸(H3BO3)与足量NaOH溶液发生酸碱中和反应的离子方程式为:H3BO3+OH-=B(OH)4-,则硼酸为一元酸,硼酸的电离方程式为H3BO3+H2O?B(OH)4-+H+.
(3)常温下,0.01mol•L-1的HNO2 溶液加水稀释的过程中,下列各项数据增大的是④⑤(填代号).
①c(H+ ) ②$\frac{c(N{O}_{2}^{-})}{c({H}^{+})}$ ③Ka(HNO2)
④$\frac{c({H}^{+})}{c(HN{O}_{2})}$ ⑤c(OH-) ⑥$\frac{c(N{O}_{2}^{-})}{c(HN{O}_{2})•c(O{H}^{-})}$
(4)如图描述的是醋酸与HNO2 在水中的电离度与浓度关系,
其中反映醋酸的是曲线乙 (填“甲”或“乙”,已知:电离度=已电离的溶质分子数/原有溶质分子总数).
(5)根据表中提供的数据可知,在溶液中能大量共存的微粒组是d (填代号).
a.H2CO3、HCO${\;}_{3}^{-}$、CH3COO-、CN- b.HCO${\;}_{3}^{-}$、CH3COOH、CN-、CO${\;}_{3}^{2-}$
c.HCN、HCO${\;}_{3}^{-}$、CN-、CO${\;}_{3}^{2-}$ d.HCN、HCO${\;}_{3}^{-}$、CH3COO-、CN
(6)设计一个现象明显、操作简便的实验方案证明HNO2酸性强于碳酸(不用叙述仪器和具体操作).
11.下列有关环境污染的叙述不正确的是( )
| A. | 使用无磷洗衣粉,可彻底解决水体富营养化问题 | |
| B. | SO2是大气污染物,可以用生石灰除去工业废气中的SO2 | |
| C. | 明矾水解产生Al(OH)3胶体粒子,可除去悬浮物 | |
| D. | 使用清洁能源是防止酸雨发生的重要措施之一 |
8.设NA表示阿伏加德罗常数的数值,下列叙述不正确的是( )
| A. | 常温常压下,1mol CO2和CO混合气体含有的碳原子数为NA | |
| B. | 在KIO3+6HI═KI+3I2+3H2O反应中,每生成 3molI2,则转移6NA个电子 | |
| C. | 78gNa2O2与足量的CO2完全反应,转移的电子总数为NA | |
| D. | 在1L0.1mol-L-1 Na2S溶液中,阴离子总数大于0.1NA |

 (填分子式),其原因是在双氧水分子中每个H原子和O原子形成一对共用电子对,O原子之间共用一对电子,这样每个原子都达到稳定结构.
(填分子式),其原因是在双氧水分子中每个H原子和O原子形成一对共用电子对,O原子之间共用一对电子,这样每个原子都达到稳定结构.