题目内容
下列实验过程中,始终无明显现象的是
A.Cl2通入FeSO4溶液中
B.CO2通入Ca(OH)2溶液中
C.将AlCl3溶液滴入 NaOH 溶液中
D.SO2通入BaCl2溶液中
D
【解析】
试题分析:A、氯气通入硫酸亚铁溶液中,则氯气与亚铁离子发生氧化还原反应,生成铁离子,所以溶液的颜色由浅绿色变为黄色,错误;B、二氧化碳与澄清石灰水反应开始有白色沉淀产生,后白色沉淀逐渐溶解,错误;C、将AlCl3溶液滴入 NaOH 溶液中,因为氢氧化钠过量,所以开始无沉淀,后有白色沉淀产生,错误;D、亚硫酸的酸性比盐酸酸性弱,所以二氧化硫通入氯化钡溶液中,无现象,正确,答案选D。
考点:考查气体与溶液反应的现象

(16分)某研究小组想探究炭与浓硝酸的反应。其实验过程如下。
操作 | 现象 |
a.用干燥洁净的烧杯取约10mL浓硝酸,加热。 | |
b.把小块烧红的木炭迅速放入热的浓硝酸中。 | 红热的木炭与热的浓硝酸接触发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧,发出光亮,上下反复跳动。 |
(1)热的浓硝酸与红热的木炭接触会发生多个化学反应。
①炭与浓硝酸的反应,说明浓硝酸具有 性。
②反应产生的热量会使少量浓硝酸受热分解,该反应的化学方程式为 。
(2)实验现象中液面上木炭迅速燃烧,发出光亮。小组同学为了研究助燃气体是O2还是NO2,设计了以下实验。

Ⅰ.制取NO2气体。
①在虚线框内画出用铜与浓硝酸制取和收集NO2的装置简图(夹持仪器略)。
②NaOH溶液的作用是吸收多余的NO2,反应生成两种物质的量相等的正盐,写出反应的的离子方程式 。
Ⅱ.探究实验。
实验操作:在空气中引燃木炭,使其燃烧并带有火焰,将带火焰的木炭伸入盛有NO2气体的集气瓶中。
实验现象:木炭在NO2气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色。
①根据实验现象写出碳与NO2气体反应的化学方程式 。
②通过实验探究,你认为上表操作b中助燃气体是什么,简述理由 。
 ;HCl(aq)与NaOH(aq) 反 应的
;HCl(aq)与NaOH(aq) 反 应的 ,则HCN在水溶液中电离的
,则HCN在水溶液中电离的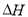 等于
等于
 B.-43.5
B.-43.5
 CO↑+CO2↑+(x+1)H2O,将生成的CO2和水蒸气除掉,即得到较纯净的CO气体。
CO↑+CO2↑+(x+1)H2O,将生成的CO2和水蒸气除掉,即得到较纯净的CO气体。
 具有健脾作用。下列有关说法正确的是
具有健脾作用。下列有关说法正确的是

