题目内容
下列条件中关于粒子组共存的评价不正确的是
选项 | 条件 | 粒子组 | 评价 |
A | 含FeCl3的溶液中 | H+、H2O2、Cl- | 会发生反应,所以不能大量共存 |
B | 室温时,pH=ll的溶液中 | Na+、ClO-、AlO2- | 能大量共存 |
C | 水电离的c(H+)=1×10-6mol/L的溶液中 | Al3+、NH4+、NO3- | 可能大量共存 |
D | 某无色溶液中 | Na+、HCO3-、OH- | 会产生CO2,所以不能大量共存 |
D
【解析】
试题分析:A.在含FeCl3的溶液中,在酸性条件下H2O2会发生分解反应产生O2和H2O,会发生任何反应,所以不能大量共存,正确;B.室温时,pH=ll的溶液是碱性溶液,在碱性溶液中,Na+、ClO-、AlO2-不会发生任何反应,能大量共存,评价正确;C.水电离的c(H+)=1×10-6mol/L的溶液中, Al3+、NH4+、NO3-不会发生任何反应,可以大量共存,评价正确;D. 某无色溶液中, 离子会发生反应:HCO3-+OH-=CO32-+H2O,因此评价有误。故选项是D。
考点:考查粒子组共存的评价正误的判断的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目



 2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示: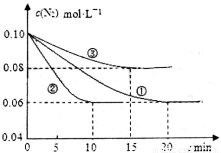
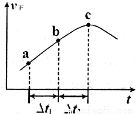
 H2O的电离平衡常数Kb=________________。
H2O的电离平衡常数Kb=________________。 CH3COCH2COH(CH3)2(aq);取相同浓度的CH3COCH3,分别在40℃和60℃时,测得其转化率
CH3COCH2COH(CH3)2(aq);取相同浓度的CH3COCH3,分别在40℃和60℃时,测得其转化率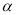 随时间变化的关系曲线(
随时间变化的关系曲线(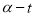 )如图所示。
)如图所示。