题目内容
12.下列有关叙述中不正确的是( )| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温材料的元素 | |
| C. | 在金属元素区域中可以寻找制备新型农药材料的元素 | |
| D. | 23592U可用作核反应堆的燃料,21H与31H可用作制造氢弹的原料 |
分析 A.在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料;
B.制备催化剂及耐高温元素为过渡元素;
C.制备新型农药材料的元素主要是:S、P、Cl等;
D.放射性元素可释放大量的能量,可用于制造核反应堆或氢弹.
解答 解:A.在金属元素和非金属元素交接区域的元素通常既具有金属性又具有非金属性,可以用来做良好的半导体材料,如硅等,故A正确;
B.在过渡元素中可以寻找制备催化剂及耐高温的元素,如:镍、铂等,故B正确;
C.在元素周期表的右上角可以寻找制备新型农药材料的元素,故C错误;
D.放射性元素可释放大量的能量,可用于制造核反应堆或氢弹,故D正确.
故选C.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置及性质为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.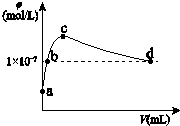 常温下,向1L pH=10的 NaOH溶液中持续通入CO2.通入的CO2的体积(V)与溶液中水电离出的OH-离子浓度(φ)的关系如图所示.下列叙述不正确的是( )
常温下,向1L pH=10的 NaOH溶液中持续通入CO2.通入的CO2的体积(V)与溶液中水电离出的OH-离子浓度(φ)的关系如图所示.下列叙述不正确的是( )
 常温下,向1L pH=10的 NaOH溶液中持续通入CO2.通入的CO2的体积(V)与溶液中水电离出的OH-离子浓度(φ)的关系如图所示.下列叙述不正确的是( )
常温下,向1L pH=10的 NaOH溶液中持续通入CO2.通入的CO2的体积(V)与溶液中水电离出的OH-离子浓度(φ)的关系如图所示.下列叙述不正确的是( )| A. | a点溶液中:水电离出的c(H+)=1×10-10mol/L | |
| B. | b点溶液中:c(H+)=1×10-7mol/L | |
| C. | c点溶液中:c(Na+)>c(CO32-)>c(HCO3-) | |
| D. | d点溶液中:c(Na+)=2c(CO32-)+c(HCO3-) |
3.某气态烃0.5mol能与1mol HCl完全加成,加成后产物分子中的氢原子又可被3mol Cl2完全取代,则此气态烃可能是( )
| A. | CH3C≡CCH3 | B. | CH2=CH2 | C. | CH≡CCH3 | D. | CH2=CHCH3 |
20.下列叙述正确的是( )
| A. | 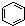 和 和 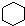 均是芳香烃, 均是芳香烃,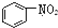 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 | |
| B. | 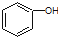 和 和 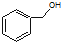 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 | |
| C. | 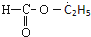 含有醛基,所以属于醛类 含有醛基,所以属于醛类 | |
| D. | 分子式为C4H10O的物质,可能属于醇类或醚类 |
7.常温下,下列对醋酸稀溶液的叙述中,正确的是( )
| A. | 将pH=a的醋酸稀释变为pH=a+1,醋酸的浓度则变为原来的$\frac{1}{10}$ | |
| B. | 将pH=a的醋酸稀释为pH=a+1的过程中,c(CH3COOH)/c(H+)$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$变小 | |
| C. | pH=a的醋酸与pH=a+1的醋酸分别中和等物质的量的NaOH溶液,二者所消耗体积比为1:10 | |
| D. | 等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,存在a+b=14 |
17. 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 非金属性:Z<T<X | B. | R与Q的电子数相差26 | ||
| C. | 气态氢化物稳定性:R<T<Q | D. | 最高价氧化物的水化物的酸性:R>T |
4.元素周期表里金属元素和非金属元素分界线附近能找到( )
| A. | 新制农药元素 | B. | 制催化剂元素 | ||
| C. | 制半导体元素 | D. | 制耐高温合金元素 |
1.A是一种常见的单质.B.C为常见的化合物.A.B.C均含有元素X.它们有如图所示转化关系(部分产物及反应条件已略去)下列有关推断正确的是( )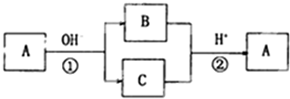
a.X元素为Al;
b.反应①和反应②互为可逆反应;
c.A可能是S或Cl2;
d.反应①和反应②一定是氧化还原反应.

a.X元素为Al;
b.反应①和反应②互为可逆反应;
c.A可能是S或Cl2;
d.反应①和反应②一定是氧化还原反应.
| A. | a和b | B. | c和d | C. | a、b、c、d | D. | b、c、d |
2.下列反应中,属于氧化还原反应同时又是吸热反应的是( )
| A. | 灼热的炭与CO2反应 | B. | 铝与稀盐酸反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 甲烷与O2的燃烧反应 |