题目内容
13.一定质量的氧化镁和氧化钙的混合物刚好与10倍质量的盐酸完全反应,求该盐酸中溶质质量分数的范围.分析 令混合物的质量为1g,则盐酸的质量为10g,假设全部为MgO,根据方程式计算消耗HCl的质量,进而计算盐酸的质量分数,再假设全部为CaO,进而计算盐酸的质量分数,盐酸的质量分数介于二者之间.
解答 解:令混合物的质量为1g,则盐酸的质量为10g,
假设全部为MgO,消耗HCl的质量为x,则:
MgO+2HCl=MgCl2+H2O
40 73
1g x
所以x=$\frac{1g×73}{40}$=1.825,盐酸的质量分数为$\frac{1.825g}{10g}$×100%=18.25%,
假设全部为CaO,消耗HCl的质量为y,则:
CaO+2HCl=CaCl2+H2O
56 73
1g y
所以x=$\frac{1g×73}{56}$=1.304g,盐酸的质量分数为$\frac{1.304g}{10g}$×100%=13.04%,
故盐酸的质量分数介于13.04%~18.25%之间,
答:故盐酸的质量分数介于13.04%~18.25%之间.
点评 本题考查化学方程式有关计算、溶液质量分数计算,关键是利用极限法确定范围.

练习册系列答案
相关题目
3.某单质甲及其化合物乙、丙、丁、戊在一定条件下发生如图所示的变化,乙可以是( )


| A. | PH3 | B. | H2S | C. | HCl | D. | NH3 |
4.下列烷烃中,既能由烯烃加氢得到也能由炔烃加氢得到的是( )
| A. | 2-甲基丙烷 | B. | 2-甲基丁烷 | C. | 2,2-二甲基丙烷 | D. | 正丁烷 |
1.元素周期表的一部分,表中的①--⑩中元素,回答下列填空:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)非金属性最强的元素是氟(填元素名称)
(3)写出①⑦对应两种元素的符号分别为N、Cl,(填元素符号)元素③⑤的最高价氧化物对应的水化物相互反应的离子方程式为Al(OH)3+OH-=AlO2-+H2O
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是(填对应化合物的化学式,下同)HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)写出确定某一溶液中含有元素⑨存在的实验操作:用洁净的铂丝蘸取少量待测试样于酒精灯外焰灼烧,透过蓝色钴玻璃观察火焰的颜色,火焰呈紫色,说明该试样含有K+.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)非金属性最强的元素是氟(填元素名称)
(3)写出①⑦对应两种元素的符号分别为N、Cl,(填元素符号)元素③⑤的最高价氧化物对应的水化物相互反应的离子方程式为Al(OH)3+OH-=AlO2-+H2O
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是(填对应化合物的化学式,下同)HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)写出确定某一溶液中含有元素⑨存在的实验操作:用洁净的铂丝蘸取少量待测试样于酒精灯外焰灼烧,透过蓝色钴玻璃观察火焰的颜色,火焰呈紫色,说明该试样含有K+.
8.下列实验方法能达到要求的是( )
| A. | 用托盘天平称量25.20gNaCl | |
| B. | 用250mL的容量瓶配制230mL的碳酸钠溶液 | |
| C. | 用25mL滴定管量取14.80mL的溶液 | |
| D. | 用pH试纸测得溶液的pH为12.6 |
2. 已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.
②有关有机物的沸点如表所示:
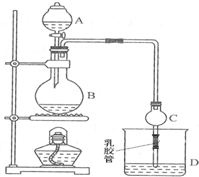
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸;B中放有乙醇、无水醋酸钠;D中放有饱和碳酸钠溶液.
试回答下列问题:
(1)浓硫酸的作用:吸水剂,催化剂,制乙酸;反应中加入过量的乙醇,目的是提高乙酸的转化率.
(2)若用同位素18O示踪法确定产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:CH3CO18OH+CH3CH2OH CH3COOCH2CH3+H218O.
CH3COOCH2CH3+H218O.
(3)仪器A的名称是分液漏斗,C的两个作用是冷却蒸汽和防止倒吸,若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-;实验完毕后,将烧杯D中溶液充分振荡、静止,现象为溶液分层,上层为无色油状液体,下层溶液颜色变浅(或褪去).
(4)从D中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇(填名称);再加无水硫酸钠,然后进行蒸馏操作就可以得到较纯净的乙酸乙酯.
 已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.②有关有机物的沸点如表所示:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
试回答下列问题:
(1)浓硫酸的作用:吸水剂,催化剂,制乙酸;反应中加入过量的乙醇,目的是提高乙酸的转化率.
(2)若用同位素18O示踪法确定产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:CH3CO18OH+CH3CH2OH
 CH3COOCH2CH3+H218O.
CH3COOCH2CH3+H218O.(3)仪器A的名称是分液漏斗,C的两个作用是冷却蒸汽和防止倒吸,若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-;实验完毕后,将烧杯D中溶液充分振荡、静止,现象为溶液分层,上层为无色油状液体,下层溶液颜色变浅(或褪去).
(4)从D中分离出的乙酸乙酯中还含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇(填名称);再加无水硫酸钠,然后进行蒸馏操作就可以得到较纯净的乙酸乙酯.
19.短周期元素A、B、C、D的原子序数依次增大,原子半径r(C)>r(D)>r(B)>r(A).B原子最外层电子数是其内层电子总数的3倍,D原子的核电荷数等于A、C原子核电荷数之和,A与C同主族.下列说法正确的是( )
| A. | 工业上常用电解熔融D的氧化物来制备D的单质 | |
| B. | 单质C、D着火,灭火时C不能用泡沫灭火器,但D可以用泡沫灭火器灭火 | |
| C. | 化合物A2B2与C2B2所含化学键类型完全相同 | |
| D. | A、B、C组成的化合物,若溶液浓度为0.01mol/L,则常温下其PH为12 |