题目内容
9.19g某二价金属氯化物中含有0.4mol Cl-,则ACl2的摩尔质量是95 g•mol-1;A的相对原子质量是24;ACl2的化学式是MgCl2.分析 根据氯离子物质的量计算ACl2的物质的量,再根据M=$\frac{m}{n}$计算其摩尔质量,进而计算A的相对原子质量,确定A的元素符号,书写化学式.
解答 解:19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的物质的量为$\frac{0.4mol}{2}$=0.2mol,ACl2的摩尔质量是$\frac{19g}{0.2mol}$=95 g•mol-1,则A的相对原子质量为95-35.5×2=24,该二价金属氯化物的化学式为MgCl2,
故答案为:95 g•mol-1;24;MgCl2.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算,有利于基础知识的巩固.

练习册系列答案
相关题目
19.在0.25mol 硫酸钠中,含有的氧原子数约为( )
| A. | 1个 | B. | 0.25个 | C. | 6.02×1023个 | D. | 5×1023个 |
20.下列原子中,最难形成离子的是( )
| A. | 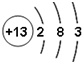 | B. |  | C. |  | D. |  |
17.现有盐酸、新制氯水、NaCl溶液和NaOH溶液,可用一种试剂将它们一一区别开,该试剂是( )
| A. | AgNO3溶液 | B. | 酚酞试液 | C. | 紫色石蕊试液 | D. | 饱和NaCl溶液 |
14.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3 g的Na完全与O2反应生成3.6 g产物时失去的电子数为0.1NA | |
| C. | 1.0 L的0.1 mol•L-1Na2S溶液中含有的S2-数为0.1NA | |
| D. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
1.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
| A. | K+、Na+、HCO3-、NO3- | B. | Ag+、K+、NO3-、Na+ | ||
| C. | H+、Mg2+、SO42-、NO3- | D. | Na+、SO42-、Cl-、ClO- |
18.国际上推广使用中国铁锅,这是因为铁锅( )
| A. | 是单质 | B. | 含碳,属混合物 | ||
| C. | 化学性质活泼 | D. | 易使食物中含人体所需的铁元素 |
19.常温时,1mol/L的CH3COOH溶液和0.1mol/L的CH3COOH溶液,其[H+]之比为( )
| A. | 1:1 | B. | 10:1 | C. | <10:1 | D. | >10:1 |