题目内容
将新制氯水逐滴滴入FeBr2溶液中,写出最初发生的反应的离子方程式,并标出电子转移的方向和数目. .
考点:氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:氯气具有氧化性,能将碘离子以及亚铁离子氧化,碘离子的还原性强于亚铁离子的还原性,所以先是发生氯气氧化亚铁离子的反应,氧化还原反应中,化合价升高值=化合价降低值=转移电子数,据此表示电子转移的情况.
解答:
解:将新制氯水逐滴滴入FeBr2溶液中,先是发生氯气氧化亚铁离子的反应,Cl2+2Fe2+=2Fe3++2Cl-,Fe的化合价升高值=Cl的化合价降低值=转移电子数=2,电子转移情况如下: ,故答案为:
,故答案为: .
.
 ,故答案为:
,故答案为: .
.
点评:本题考查学生氧化还原反应中电子转移的表示方法以及反应的先后顺序知识,注意知识的归纳和整理是关键,难度不大.

练习册系列答案
相关题目
下列各对物质中属于同分异构体的是( )
| A、612C和613C |
| B、O2和O3 |
| C、(CH3)2CHCH2CH3和C(CH3)4 |
| D、H2C(CH3)2和CH3CH2 CH3 |
 如图,小烧杯放在一块沾有水的玻璃片上,加入氯化铵固体与氢氧化钡晶体[Ba(OH)2?8H2O)],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可知( )
如图,小烧杯放在一块沾有水的玻璃片上,加入氯化铵固体与氢氧化钡晶体[Ba(OH)2?8H2O)],并用玻璃棒搅拌,玻璃片上的水结成了冰.由此可知( )| A、该反应中,化学能转变成热能 |
| B、反应物的总能量低于生成物的总能量 |
| C、氯化铵与氢氧化钡的反应为放热反应 |
| D、反应的热化学方程式为 2NH4Cl+Ba(OH)2→BaCl2+2NH3?H2O-Q |
某化学兴趣小组学习原电池知识后,决定用其原理,尝试利用铁粉、活性炭、无机盐等物质开发产品.小组提出的设想或对原理的理解不正确的是( )
| A、打算制成小包装用于糕点的脱氧剂 |
| B、利用反应放出热量的原理制成暖宝宝 |
| C、调整电池结构,可降低温度,可用于延长糕点保质期 |
| D、正极的电极反应为:2H2O+O2+4e-=4OH- |
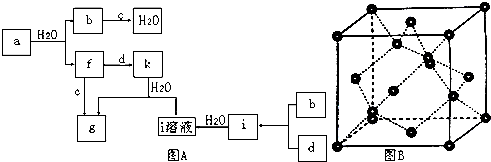



 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献. 某课外活动小组用如图装置进行实验,试回答下列问题.
某课外活动小组用如图装置进行实验,试回答下列问题.